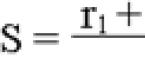Геморрагическая лихорадка с почечным синдромом характеризуется повышенной сосудистой проницаемостью и нарушениями коагуляции. Было признано, что человеческие эндотелиальные клетки, выделенные как из взрослой, так и внутриутробной вены, очень восприимчивы к инфекции ГЛПС. Однако инфицирование in vitro ГЛПС не вызывает какого-либо заметного цитопатического эффекта, о чем свидетельствуют как фазовая микроскопия, так и электронная микроскопия. Таким образом, хантавирус считается нецитопатогенным вирусом, который нацелен прежде всего на сосудистые эндотелиальные клетки.
Патогенез в основном неизвестен, но результаты нескольких исследований показали, что иммунные механизмы играют важную роль. После заражения происходит образование выраженных цитокинов, активация калликреин-кининов, активация пути комплемента или повышение уровня циркулирующих иммунных комплексов. Эти компоненты играют важную роль во время лихорадочной и гипотензивной стадий. Клинически значимыми признаками заболевания являются повреждение сосудистого эндотелия, расширение капилляра и утечка.
Активный ответ часто является признаком тяжелой болезни. Т-клеточная активация происходит очень рано в ходе лихорадки и связана с абсолютным увеличением числа нейтрофилов, моноцитов, В-клеток и CD8 + (супрессорных) Т-клеток. Количество хелперных Т-клеток не увеличивается, что приводит к уменьшению отношения Т-клеток-помощников-супрессоров. Вирус культивировали из В-клеток и моноцитов, но не из Т-клеток. Поэтому активация Т-клеток является ответом на инфекцию других типов клеток, а не следствием прямой вирусной инфекции. Интерферон-гамма-продуцирующие Т-клетки могут помочь снизить риск прогрессирования ОПН.
Возможная роль иммунных комплексов также была предложена после демонстрации иммунных комплексов в сыворотке, на поверхности эритроцитов и тромбоцитов, в клубочках, в почечных канальцах и в моче. Активация классических и альтернативных путей комплемента происходит также при лихорадке. Активируя комплемент и вызывая высвобождение медиатора из тромбоцитов и воспалительных клеток, иммунные комплексы могут вызывать сосудистую травму, которая является отличительной чертой болезни.
Некоторые исследователи предположили, что лихорадка является прежде всего аллергическим заболеванием. Это основано на обнаружении раннего появления специфического иммуноглобулина Е (IgE), наличия иммунных комплексов IgE и благоприятных эффектов терапии, направленных на ингибирование аллергических путей.
Повышенная вирусная нагрузка, вероятно, приведет к более тяжелому клиническому результату. Нагрузка ГЛПС РНК в плазме у пациентов на ранних стадиях ГЛП связана с тяжестью заболевания. Тесная корреляция между вирусной нагрузкой и тяжестью заболевания также была обнаружена в случаях с вирусом Добрава-Белград (Dobrava-Belgrade).
Было высказано предположение, что клеточная проницаемость индуцируется хантавирусом. Анализ образцов биоптата почки у пациентов, инфицированных хантавирусом, показал, что экспрессия и локализация белка ZO-1 с плотным соединением были изменены по сравнению с образцами биопсии почек у неинфицированных индивидуумов, при которых инфекция поражала как трубчатые, так и гломерулярные клетки. Снижение клубочкового ZO-1 коррелирует с тяжестью болезни, вызванной клубочковой дисфункцией.
VE-кадгерин был обнаружен на ранних стадиях первичного легкого заболевания человека, эндотелиальная клетка была инфицированна вирусом Andes. Сообщалось, что повышенный секретируемый сосудистый эндотелиальный фактор роста и сопутствующий снижаются. Исследование также показало, что активная репликация вируса может привести к повышению проницаемости и снижению целостности барьера эндотелиальных клеток.
В другом исследовании было установлено, что связь между сосудистым эндотелиальным фактором роста с рецептором может приводить к диссоциации сосудистого эндотелиального фактора роста -R2 из VE-кадгерина, активации VE-кадгерина, интернализации и деградации, это добавляет сосудистый эндотелиальный фактор роста к эндотелиальным клеткам, инфицированным Хантавирусом.
Как заражаются
Хантавирусы переносятся и передаются грызунами. Люди могут заразиться этими вирусами и развивать ГЛПС после воздействия с запахом мочи, помета или слюны инфицированных грызунов или после контакта с пылью из их гнезд.

Передача может также произойти, когда инфицированная моча или другие материалы непосредственно попадают на поврежденную кожу или на слизистые оболочки глаз, носа или рта. Кроме того, люди, которые работают с живыми грызунами, могут подвергаться воздействию хантавирусов через укусы грызунов, когда они являются инфицированными. Передача от одного человека к другому может произойти, но крайне редко.
Симптомы
Лихорадка обычно развиваются в течение 1 — 2 недель после взаимосвязи с инфекционным материалом, но в редких случаях требуется 8 недель для развития.
Начальные симптомы начинаются внезапно, к ним относятся: боли головные, в животе и спине, лихорадку, озноб, тошноту и помутнение зрения. У людей может быть покраснение лица, воспаление или покраснение глаз или сыпь.
Более поздние симптомы могут включать низкое кровяное давление, острый шок, утечку сосудов и острую почечную недостаточность, которая может вызвать сильную перегрузку жидкостью.
Инфекции Хантаан и Добрава обычно вызывают серьезные симптомы, а инфекции Сеула, Сааремаа и Пуумала обычно более умеренные. Полное выздоровление может занять недели или месяцы.
Диагностика
Несколько лабораторных тестов используются для подтверждения диагноза ГЛПС у пациентов с клинической историей, совместимой с заболеванием. Такие пациенты, как установлено, имеют ГЛПС, если у них есть:
- результаты серологических тестов, положительные для инфекции хантавируса;
- доказательства наличия антигена хантавируса в ткани при иммуногистохимическом окрашивании и исследовании микроскопа
- доказательства последовательности хантавирусной РНК в крови или ткани.
 Хантавирусные инфекции могут проявляться клинически нехарактерными и мимическими синдромами, такими как острая боль в животу. Ненужные операции с иногда опасными для жизни осложнениями могут быть следствием неверно истолкованных симптомов. Аналогичные случаи имели место в скандинавских странах и в России. Повышение осведомленности о хантавирусных инфекциях в Скандинавии резко сократило ненужные хирургические вмешательства. Это может быть более трудным достижением в Западной и Центральной Европе, поскольку число случаев ГЛПС намного меньше.
Хантавирусные инфекции могут проявляться клинически нехарактерными и мимическими синдромами, такими как острая боль в животу. Ненужные операции с иногда опасными для жизни осложнениями могут быть следствием неверно истолкованных симптомов. Аналогичные случаи имели место в скандинавских странах и в России. Повышение осведомленности о хантавирусных инфекциях в Скандинавии резко сократило ненужные хирургические вмешательства. Это может быть более трудным достижением в Западной и Центральной Европе, поскольку число случаев ГЛПС намного меньше.
Серология по-прежнему остается первой в выборе диагностики хантавирусных инфекций. Большинство серологических анализов созданы для диагностики групп хантавирусов, а не конкретных серотипов. Из-за серологической перекрестной реактивности между серотипами таких групп положительный результат может проявиться в тестах против любого из родственных антигенов. Любая лаборатория, предлагающая диагностику хантавируса, должна удовлетворять минимальным требованиям для критической интерпретации своих тестов и должна обращаться в справочный центр за консультацией в критических и сомнительных случаях.
Проблемы с контролем качества и оценкой тестов могут усугубляться фактами, что инфекции редки и несколько серотипов могут циркулировать.
Лечение
Поддерживающая терапия является основой ухода за пациентами с хантавирусными инфекциями. Уход включает:
- тщательное управление уровнями жидкости (гидратация) и электролит (например, натрия, калия, хлорида);
- поддержание правильного уровня кислорода и артериального давления;
- соответствующее лечение любых вторичных инфекций.
Диализ может потребоваться для коррекции тяжелой перегрузки жидкостью. Показано, что внутривенный рибавирин, противовирусный препарат, уменьшает заболеваемость и смертность, если они используются на ранних стадиях заболевания.
Тромбоцитарные переливания могут использоваться в тяжелых случаях с тромбоцитопенией и явными кровотечениями. Симптоматическое лечение также необходимо для пациентов с головной болью и болями в спине.
Непрерывная заместительная почечная терапия стала важной и широко используемой терапией для пациентов с критической, сопровождающихся повреждением муртиоргана, отеком легких, перегрузкой жидкости, тяжелыми нарушениями электролитов и церебропатией.
Сложным и опасным является заболевание геморрагическая лихорадка с почечным синдромом (эбола, болезнь Марбурга). Его эпидемиология представляет собой отклонения зоонозного характера, т. е. распространяется животными. Геморрагическая лихорадка имеет разные пути поражения, а под влияние заболевания попадает практически весь организм ― поражаются почки и печень, оказывается разрушительное действие на сердечно-сосудистую систему, вызываютсяет отклонения в гемодинамике. Данная болезнь протекает тяжело и характеризуется осложнениями состояния пациента - может стать причиной токсического шока и закончиться смертью.
Характеристика возбудителя
Геморрагическая лихорадка с почечным синдромом является вирусом. Это было доказано научным исследованием в 1944 г. Однако изучить возбудители болезни удалось гораздо позже. Им является бактерия, которая содержится в легких южнокорейского грызуна. Называется этот возбудитель - Хантанаан. На сегодняшний день болезнь ГЛПС относят к группе, так называемых бунья-инфекций. Патоген представляет собой сферу диаметром от 85 до 120 нм. Его дифференциальный геном подразделен на три части, которые обозначают латинскими буквами L, M, S. Инфекционные размножения происходят через цитоплазму зараженных молекул. Воздействию эболы подвержены многие клетки: печени, почек, легких, слюнных желез. При очаге ГЛПС происходит антигенная реакция.
Геморрагическая адаптация
Классификация ГЛПС разнообразна. Уже известно более 25-ти подвидов бактериофагов. Они развиваются в разных странах и регионах. Проблема охватывает территории Японии, Китая, России, КНДР, Южной Кореи и Дальнего Востока. Классическим переносчиком считается мышь рыжая полевка. Болезнь Марбурга легко адаптируется к окружающей среде, выживает при средней температуре ― 4―20 градусов. При взятии проб крови, живет в сыворотке до 4-х дней, после чего «засыпает». Снова проявляет активность при увеличении тепла до 50-ти градусов. Эбола чувствителен к кислотной среде, хлороформу, бензолу, ацетону, эфиру и ультрафиолетовым лучам.
Этиология заболевания
 Источником заражения в Европе считаются грызуны: полевка, крысы, хомяки. Ареалом для выживания и размножения переносчиков считаются лесостепные зоны, предгорные и речные долины, лесостепи. Заразиться лихорадкой с почечным синдромом можно:
Источником заражения в Европе считаются грызуны: полевка, крысы, хомяки. Ареалом для выживания и размножения переносчиков считаются лесостепные зоны, предгорные и речные долины, лесостепи. Заразиться лихорадкой с почечным синдромом можно:
- через пыль, вдыхая остатки продуктов жизнедеятельность зараженных грызунов;
- путем попадания испражнений животных в рот (попадание их в еду, напитки);
- через кожу при касании к инфицированным предметам, животным, экскрементам, которые могут находиться в корме, сене, хворосте.
Существуют различные пути попадания геморрагических молекул в кровь, в зависимости от места передачи:
- Лесной - заболеваемость наиболее высока. Бактериофаг попадает в организм во время прогулки по лесу, при собирательстве грибов и ягод.
- Бытовой - возможность передачи заболевания в жилой зоне обусловлена проникновением туда переносчиков.
- Производственный - объясняется проведением работ, связанных с большим количеством пыли и полевыми работами: бурение, закладка нефтепроводов.
- Садово-огородный - заразиться можно через землю, где находятся инфицированные фекалии грызунов.
- Лагерный - заражение происходит во время отдыха в общественных учреждениях, находящихся в природных условиях.
- Сельскохозяйственный - опасность носит сезонный характер и обусловлена проведением хозяйственных работ.
Патогенез и его особенности
После перенесенной инфекции формируется прочный иммунитет. Повторные заболевания у одного человека не встречаются. Патогенез заболеваемости еще мало изучен. Поэтому существует только приблизительная лабораторная структура развития бактерий. Известны прогрессирующие стадии ГЛПС, по которым происходит постепенно развитие недуга. Ниже приведены 5 основных этапов.
Заболеваемость и первые проявления

 Геморрагическая лихорадка распространяется с помощью слизистой оболочки органов дыхания, пищеварения и покровы кожи. Далее инфекция размножается в СМФ и лимфатических узлах. Инфекционные молекулы токсично воздействуют на сосуды и ЦНС. На этом этапе заканчивается инкубационный период, болезнетворные тела проникают в кровеносную систему.
Геморрагическая лихорадка распространяется с помощью слизистой оболочки органов дыхания, пищеварения и покровы кожи. Далее инфекция размножается в СМФ и лимфатических узлах. Инфекционные молекулы токсично воздействуют на сосуды и ЦНС. На этом этапе заканчивается инкубационный период, болезнетворные тела проникают в кровеносную систему.
Аллергия, интоксикация и поражение иммунитета
Токсико-аллергические и иммунологические реакции. При атаке инфекционных организмов, защитные клетки пытаются нейтрализовать деструктивное воздействие. По этой причине образуются клеточные скопления или комплексы - ИК. Если действие геморрагической лихорадки не удалось остановить, ИК попадают в соединительные ткани и органы. Это оказывает разрушительное действие на вегетативные центры и сосуды. Вследствие этого развивается ряд функциональных отклонений: микротромбоз, понижение сосудистого тонуса, плазморея, диатез, ОПН.
Патологии обменных процессов
Развивающаяся инфекция приводит к отечности в надпочечниках, почках, печени, паренхиме. Возможно развитие дистрофии органов и клеточный некроз. Такие изменения ведут к новым заболеваниям - гипоксии, ацидозу в тканях, гиповолемии, нарушению кровообращения, повреждению жизненно важных центров в теле человека. Больше всего подвержена стрессу почечная система: происходит сбой клубочковой фильтрации с проявлением олигурии, азотемии, протоанурии. Эта стадия может стать угрозой для жизни пациента, поскольку происходят серьезные осложнения в виде коллапса, уремии, паралича, разрыва почек.
Восстановление
 Полиурия - увеличенное образование мочи.
Полиурия - увеличенное образование мочи.
С наступлением восстановительной стадии и формируется иммунитет к заболеванию. Из-за изменений состояния организма увеличивается количество вырабатываемой мочи - полиурия, снижается способность всасывания в кровь полезных веществ. Как следствие, уменьшается количество продуктов обмена, содержащихся в сыворотке крови, что дает возможность постепенного восстановления функций почек в период до 5-ти лет.
Какова симптоматика протекания заболевания?
Инкубация и геморроидальная лихорадка
Симптомы данной болезни характеризуются определенной цикличностью и проявляются в разные периоды.
Время инкубации вируса - варьируется. Период протекает от недели до полутора месяца. Средний срок - около 2-х недель. Начальный этап - длиться не более 3-х дней. Наблюдаются головные боли, ломота, слабость и озноб. В первую очередь у пациента проявляется геморрагическая лихорадка, когда жар поднимается до 40-ка градусов. Она держится около 2-х недель. Наиболее сильная лихорадка наблюдается в первой половине дня. Кроме того, присутствуют признаки отравления - жажда, осушение полости рта, снижение аппетита, нарушения сна и зрения. Происходят нарушения в мышцах и суставах, на языке виден налет, наблюдается покраснение слизистой оболочки глаз.
Олигурический синдром
 Период снижения количества выделяемой мочи - наблюдается после лихорадки. Проявления наблюдаются в течение 10-ти суток. На этом этапе перестает лихорадить, но облегчения это не приносит. Начинают беспокоить ломота и боли в пояснице. Тяжелые случаи вируса Марбурга могут сопровождаться рвотным рефлексом, а болевые ощущения распространяются на область пищеварения. Общий биохимический анализ крови на ГЛПС покажет повышение уровня калия, мочевины, хлоридов, кальция, креатина. Кроме того, на коже появляются высыпания - в районе подмышек, груди и плеч. Могут открыться кровотечения, как внешние (кровь из носа), так и внутренние (кровоизлияния в органах ЖКТ). Развивается почечная и печеночная недостаточность.
Период снижения количества выделяемой мочи - наблюдается после лихорадки. Проявления наблюдаются в течение 10-ти суток. На этом этапе перестает лихорадить, но облегчения это не приносит. Начинают беспокоить ломота и боли в пояснице. Тяжелые случаи вируса Марбурга могут сопровождаться рвотным рефлексом, а болевые ощущения распространяются на область пищеварения. Общий биохимический анализ крови на ГЛПС покажет повышение уровня калия, мочевины, хлоридов, кальция, креатина. Кроме того, на коже появляются высыпания - в районе подмышек, груди и плеч. Могут открыться кровотечения, как внешние (кровь из носа), так и внутренние (кровоизлияния в органах ЖКТ). Развивается почечная и печеночная недостаточность.
Проявление полиурии
Затем наступает увеличение выделяемой жидкости, он протекает до месяца. На этом этапе проявления практически пропадают и пациенту становиться легче. Присутствует полиурия, когда моча выделяется в больших объемах ― до 10 л. Работа печени и почек постепенно восстанавливается, содержание веществ в крови нормализуется. В течение месяца процесс мочеиспускания приходит в норму, остается только легкое недомогание, частые позывы к мочеиспусканию.
Восстановление
Далее начинается период восстановления: больной выздоравливает, функции приходят в норму, а признаки больше не проявляются. Эта стадия длится от года до 3-х. Происходит проявление остаточных признаков. Обычно, их делят на 3 группы:
- астения - сопровождается отсутствием аппетита, слабостью, головокружениями;
- отклонения в эндокринной и нервной системах - проявляются повышенным потоотделением, зудом на коже, жаждой, болями у основания позвоночника, импотенцией; Сильный жар у ребенка держится в течение недели.
Клиника ГЛПС у детей проявляется в любом возрасте, даже у новорожденных. У младшего поколения зачастую отсутствуют начальные симптомы развития вируса, а проявляются сразу в острой форме. Сильный жар держится в течение недели, он сопровождается сильными головными болями, слабостью, сонливостью, общим недомоганием, рвотными позывами. Болезненные ощущения в спине появляются практически сразу, постепенно переходя в область живота.
Первое описание ее было сделано в 1935 году на Дальнем Востоке, затем выяснилось, что она распространена в Московской, Тульской, Ярославской, Самарской, Тверской областях, Предуралье. Заболевание характеризуется избирательным поражением кровеносных сосудов почек.
Инфекция вызывается вирусами рода Хантавирусов, их переносчиками выступают лесные и полевые мыши. Вирус выделяется в окружающую среду со слюной и испражнениями грызунов, заражение происходит при вдыхании воздуха, загрязненного частицами высохших выделений мышей, возможен и пищевой путь заражения - через продукты.
Люди достаточно восприимчивы к заболеванию, но для окружающих больной человек не представляет опасности. Перенесенная инфекция оставляет после себя стойкий пожизненный иммунитет.
Что происходит?
Инкубационный период составляет 7-46 дней. Возбудитель ГЛПС поражает кровеносные сосуды. В результате их проницаемость повышается, происходит выход плазмы - жидкой части крови - в окружающие ткани. Сама же кровь сгущается, нарушается работа ее свертывающей системы. В большей степени страдают сосуды почек, развивается острая почечная недостаточность, возможет даже разрыв почки. Помимо этого характерны и общие реакции организма на вторжение вируса - высокая температура (лихорадка), интоксикация и другие.
Болезнь обычно начинается внезапно, с острых и интенсивных головных болей преимущественно в надглазничных и височных областях. Одновременно - в течение нескольких часов - нарастает температура тела. Она быстро достигает 38-40°С. К концу первого дня многие больные отмечают снижение остроты зрения. Отмечается также тошнота, доходящая до рвоты, часто появляется икота.
Температура удерживается в течение 3-5 дней, затем постепенно снижается, но состояние больных не улучшается, а наоборот. В это время развивается почечный синдром, характеризующийся болями в поясничной области и животе, снижением количества выделяемой мочи, в тяжелых случаях возможна анурия (полное отсутствие мочи).
К концу второй недели болезни рвота прекращается, исчезают боли в пояснице и животе, количество суточной мочи может достигать 5 и более литров. Переход в период выздоровления отмечается обычно к 4-ой неделе заболевания.
Диагностика
В первый период болезни распознать ГЛПС бывает сложно. От острых респираторных заболеваний ее можно отличить по отсутствию насморка, кашля и других симптомов поражения дыхательных путей, а от кишечных инфекций - поздним появлением болей в животе и рвоты, которые с течением болезни только усиливаются.
Основной диагностический признак - резкое уменьшение количества мочи и ухудшение состояния больного после нормализации температуры тела. Возможно также лабораторное подтверждение диагноза ГЛПС.
Лечение
Лечение проводится в условиях инфекционного отделения. Назначается противовоспалительное лечение, нормализация выделения мочи. Не применяются препараты, усиливающие поражение почек.
Профилактика
Сводится к мерам по защите от грызунов при нахождении на природе. Так, следует избегать зарослей травы, а запасы пищи необходимо хранить в недоступных для мышей местах и таре.
Геморрагическая лихорадка с почечным синдромом (ГЛПС) – это острое вирусное зоонозное природно-очаговое заболевание, которое сопровождается сильным повышением температуры тела и почечной недостаточностью. Вызывают его РНК-вирусы Hantaan – Хантаан, распространённый в основном на востоке, и Puumala – Пуумала, локализующийся в западных районах Европы.
Первый вирус более опасный, летальность при заболеваемости ГЛПС составляет до 20%. Второй – вызывает заболевание с менее тяжёлым течением и летальностью до 2%. На Дальнем Востоке встречаются случаи ГЛПС, вызванные вирусом Seoul – Сеул. Такое заболевание переносится в лёгкой форме.
Причины и патогенез
Вирусы изначально попадают в организм грызунов-переносчиков (домашние и полевые мыши, крысы, тушканчики, летучие мыши), которые заражают друг друга воздушно-капельным путём и переносят ГЛПС в латентной форме, то есть не болеют. Человек может заразиться следующими способами:
- контактным: при соприкосновении с грызунами, их испражнениями;
- воздушно-пылевым: вдыхание воздуха, в котором находятся мельчайшие частички высушенных испражнений грызунов;
- фекально-оральным: проглатывание грязной пиши, содержащей частицы экскрементов грызунов, во время еды.
Люди восприимчивы к возбудителю в 100% случаев. Больше всего страдают от геморрагической лихорадки с почечным синдромом мужчины от 16 до 70 лет.
Для геморрагической лихорадки с почечным синдромом (ГЛПС) характерна сезонность и наличие эндемичных территорий. Пики заболеваемости отмечаются с начала лета до начала зимы. В России самая большая частота заболеваемости геморрагической лихорадкой с почечным синдромом зафиксирована в Татарстане, Удмуртии, Башкортостане, а также в Самарской и Ульяновской областях.
Частые случаи заболеваемости регистрируются в Поволжье и на Урале в широколиственных зонах. В меньшей степени случаи ГЛПС зафиксированы в восточносибирском регионе.
Перенесённая единожды геморрагическая лихорадка с почечным синдромом даёт стойкий иммунитет на всю жизнь.
Вирус в организме человека оседает на слизистых оболочках дыхательной и пищеварительной системы. Затем он размножается и проникает в кровь. В этот период у пациента наблюдается интоксикационный синдром вследствие проникновения в кровеносное русло инфекции.
В дальнейшем Хантаан локализуется на внутренней стенке сосуда и нарушает его целостность. У больного возникает геморрагический синдром. Вирус выводится из организма мочевыделительной системой, поэтому происходит:
- поражение почечных сосудов;
- воспаление и отёк тканей почек;
- развитием острой почечной недостаточности.
Этот период ГЛПС особенно опасен и характеризуется неблагоприятным летальным исходом. В благоприятных случаях начинается обратный процесс: рассасывание геморрагий, восстановление выделительных функций почек. Длительность восстановительного периода при ГЛПС может составлять от одного до трёх лет.
Виды и типы
В настоящее время не существует единой принятой классификации ГЛПС.
В зависимости от того, на какой территории зарегистрировано заболевание, выделяют следующие виды ГЛПС:
- ярославская форма лихорадки;
- закарпатская форма ГЛПС;
- уральская форма ГЛПС;
- тульская форма ГЛПС;
- дальневосточная форма ГЛПС;
- корейская форма лихорадки и др.
В зависимости от вида РНК-вируса, вызвавшего ГЛПС, выделяют:
- западный тип ГЛПС – вызван вирусом Puumala; тяжёлое течение в 10%, сопровождающее олигоанурией и геморрагическим симптомом. Смертность – 1-2%; распространение на европейской территории;
- восточный тип ГЛПС вызван вирусом Hantaan. Очень тяжёлое течение в 40-45% случаев, сопровождающееся синдромом острой почечной недостаточности и геморрагическим синдромом. Летальность – около 8%, распространение в основном на сельскохозяйственных территориях Дальнего Востока;
- ГЛПС, вызван серотипом Seoul. Течение относительно лёгкое в 40-50%, сопровождается развитием гепатита и нарушений со стороны дыхательной системы. Распространён среди городских жителей на Дальнем Востоке.

В зависимости от зоны или территории, на которой происходит инфицирование ГЛПС:
- в лесу (лесной тип ГЛПС) – во время сбора грибов и ягод при контакте с заражёнными высушенными фекалиями больных грызунов;
- в быту (бытовой тип ГЛПС);
- на производстве (производственный тип ГЛПС) – работа в лесной зоне, на нефтепроводах в тайге, на буровых установках;
- на приусадебном участке (дачный тип ГЛПС);
- на отдыхе в палаточных городках, в лагерях и т. п.;
- на сельскохозяйственных полях.
Стадии и симптомы заболевания
Симптоматическая специфика заболевания меняется в зависимости от стадии ГЛПС. Стадий всего четыре и для них характерно цикличное чередование. Другими словами, через какое-то время после четвёртой стадии снова наступает первая и т. д.
Ацикличностью характеризуется только течение ГЛПС, вызванной серотипом Сеул.
Инкубационный период при геморрагической лихорадке с почечным синдромом имеет длительность около 2-4 недель, в это время симптомы не проявляются.
- Начальный или лихорадочный период ГЛПС – не больше 7 дней, чаще всего 3-4 дня. Начинается остро: температура тела больного в первый день достигает 38,5-40,5̊ С. Человек ощущает головные, спинные и мышечные боли, общее недомогание, сухость в ротовой полости и жажду, мелькание перед глазами «мошек» и затуманенность изображения. В этот период могут отмечаться небольшие кровоизлияния на слизистой оболочке нёба и склере.
- Олигурический период ГЛПС – около недели. Температура тела понижается, но состояние становится хуже. У больного появляются кровотечения из носа, кровоподтёки на теле, изъязвленные склеры. В области груди, в подмышечных впадинах и на нижних конечностях образуется красная сыпь, которая является проявлением многочисленных разрывов капилляр. Отмечается усилие жалоб на боли в спине и животе. Снижается суточный объём мочи. Иногда диагностируется увеличение в размерах печени.
- Полиурический период ГЛПС – начинается на 10-13 сутки. Суточный объём мочи увеличивается до 6 литров. Обнаруживается низкая плотность мочи при отсутствии её колебаний, что является признаком острой почечной недостаточности.
- Реконвалесцентный период ГЛПС – самый длительный, начинается на 20-22 сутки и продолжается около полугода. Характеризуется улучшением общего состояния пациента и нормализацией диуреза. Восстановление при лёгких степенях тяжести ГЛПС наблюдается через 1 месяц, а при среднем течении – только через 5-6 месяцев. У больных, перенесших тяжёлую форму ГЛПС, астенический синдром проявляется всю жизнь.

Симптомы различных синдромов геморрагической лихорадки
Три основных синдрома заболевания имеют различную степень проявления в зависимости от тяжести ГЛПН:
- интоксикационный;
- геморрагический;
- почечный
Геморрагическая лихорадка с почечным синдромом лёгкой степени тяжести проявляется:
- трёх-, четырёхдневным повышением температуры больного до 38 0С;
- небольшими головными болями;
- временной агнозией;
- точечными кровоизлияниями;
- отмечается снижение диуреза;
- лабораторно в моче выявляется повышение уровня белка, мочевины;

Средняя степень ГЛПС характеризуется:
- пяти-, шестидневным повышением температуры тела до 39-40 0С;
- достаточно сильной цефалгией;
- кровоизлияния на коже и слизистых оболочках носят множественный характер;
- периодически у больного появляется рвота с кровью;
- увеличивается частота сердечных сокращений, что является появлением начальной стадии инфекционно-токсического шока;
- олигурия у пациентов держится около 3-5 суток;
- лабораторно в моче отмечается повышение уровня белка, креатинина, мочевины.
Тяжёлая степень ГЛПС сопровождается:
- продолжительным (более 8 суток) повышением температуры тела больного до 40-41 оС;
- многократной рвотой с кровью;
- системными геморрагиями кожи и слизистых.
Признаки инфекционной интоксикации:
- расстройства пищеварения;
- слабость;

Со стороны мочевыделительной системы:
- портеинурия;
- олигурия;
- гематурия;
- повышение уровня мочевины и креатинина.
ГЛПС подвержены дети всех возрастов, даже грудные. Течение болезни у них отличается очень острым началом, которому не предшествуют симптомы. Дети становятся слабыми и плаксивыми, больше лежат, жалуются на головную и спинную боль в области поясницы уже на первой стадии заболевания.
Диагностика геморрагической лихорадки
Для постановки точного диагноза ГЛПС важно учитывать эпидемиологический анамнез у пациента, наличие клинических проявлений заболевания, данные лабораторных и серологических исследований. При необходимости может потребоваться проведение ФГДС, УЗИ, компьютерной томографии, рентгенологического исследования.
При наличии симптомов геморрагической лихорадки с почечным синдромом у пациента уточняется возможность контактов с полевыми мышами и другими грызунами, которые являются переносчиками заболевания. Клиническая картина ГЛПС характеризуется лихорадкой в течение 7 дней, покраснением кожи головы и шеи. Кроме этого, наблюдается геморрагический синдром и симптомы почечной недостаточности при понижении температуры тела.

Диагностику ГЛПС проводят по следующим лабораторным и серологическим исследованиям:
- общий анализ мочи и крови;
- реакция непрямой иммунофлюоресценции;
- радиоиммунный анализ;
- реакция пассивной гемагглютинации в парных сыворотках.
В крови больного диагностируется лейкопения во время начального периода, сопровождающего стойким повышением температуры тела. На следующих стадиях ГЛПС отмечается повышение СОЭ, нейтрофильный лейкоцитоз и тромбоцитопения, появление в крови клеток плазмы. Появление у пациента антител к вирусу диагностируется на 7-8 сутки заболевания, максимум их наблюдается на 13-14 сутки.
Геморрагическая лихорадка с почечным синдромом схожа по течению с другими заболеваниями, которые характеризуются повышением температуры тела: брюшной тиф, клещевые риккетсиозы и энцефалиты, лептоспирозы и простой грипп. Следовательно, при выявлении ГЛПС важна дифференциальная диагностика.
Лечение заболевания
Лечение больных геморрагической лихорадкой с почечным синдромом проводится только в инфекционном отделении стационара. Пациенту обязательно предписывается постельный режим, особенно в период болезни с гипертермией. Показано питание, богатое углеводами с исключением мяса и рыбы (диетический стол №4).
Лечение, направленное на устранение причины, вызвавшей ГЛПС, может дать положительный эффект только в первые 5 суток болезни.
Назначают медикаментозное лечение препаратов, которые ингибируют синтез РНК. Кроме этого, пациенту проводят терапию человеческим иммуноглобулином, перорально и ректально назначают альфа-интерфероны, индукторы интерферонов.

Геморрагическая лихорадка с почечным синдромом характеризуется множественными патогенными изменениями органов. Следовательно, терапия направлена также на устранение этих патогенных изменений, вызванных синдромом интоксикации и почечной недостаточности, геморрагическим синдромом. Больным назначаются:
- глюкоза и полиионные растворы;
- препараты кальция;
- аскорбиновой кислоты;
- эуфиллин;
- папаверин;
- гепарин;
- мочегонные препараты и т.д.

Также больным проводят лечение, направленное на снижение чувствительности организма к вирусу. Симптоматическое лечение ГЛПС включает купирование рвоты, болевых симптомов, восстановление деятельности сердечно-сосудистой системы.
При тяжелых формах ГЛПС показан гемодиализ и другие способы коррекции гемодинамики и нарушений системы свёртывания крови.
В восстановительном периоде ГЛПС больной нуждается в общеукрепляющей терапии, полноценном питании. Пациенту назначается также физиотерапия, лечебно-физкультурный комплекс и массаж.
Прогноз и профилактика
Если вовремя пациенту проводится адекватная терапия (на стадии лихорадки), то наступает выздоровление.
Однако в большинстве случаев после перенесения геморрагической лихорадки с почечным синдромом наблюдаются остаточные явления на протяжении полугода. К ним относят:
- астенический синдром (слабость, быстрая утомляемость);
- болезненные проявления со стороны почек (отёчность лица, сухость во рту, поясничные боли, полиурия);
- нарушения работы эндокринной и нервной системы (плевриты, гипофизарная кахексия);
- развитие кардиомиопатии вследствие перенесённого инфекционного заболевания (одышка, сердечные боли, учащённое сердцебиение);
- очень редко развивается хронический пиелонефрит.

Люди, переболевшие ГЛПС, нуждаются в наблюдении у нефролога, офтальмолога и инфекциониста каждые три месяца в течение одного года.
Тяжёлое течение данного заболевания опасно риском развития осложнений, которые в 7-10% случаев приводят к летальному исходу.
Профилактика геморрагической лихорадки с почечным синдромом заключается в соблюдении мер личной гигиены, особенно это касается людей, которые проживают на территориях-эндемиках. После пребывания в лесах, на полях, на приусадебных участках (на территориях распространения грызунов) нужно тщательно мыть руки, продезинфицировать одежду. Необходимо хранить пищевые продукты в герметичной упаковке.
Чтобы избежать заражения геморрагической лихорадкой с почечной недостаточностью нужно пить только прокипячённую воду.
При работе в пыльных условиях (на поле, в амбаре и т. п.) надевать на лицо маску или респиратор для предотвращения заражения воздушным путем.
Ни в коем случае не нужно брать в руки, трогать или гладить грызунов. На природно-очаговых территориях нужно проводить своевременную дератизацию, тщательную уборку жилых помещений.
Вакцинация от ГЛПС невозможна вследствие отсутствия разработок.
Геморрагические лихорадки (А90-А99) - группа природно-очаговых вирусных заболеваний с симптомами геморрагического диатеза, лихорадкой, интоксикацией и весьма частым поражением внутренних органов, особенно почек.
Группа геморрагических лихорадок насчитывает 11 нозологических форм (желтая лихорадка, геморрагическая лихорадка Крым-Конго- Хозер, омская геморрагическая лихорадка, геморрагическая лихорадка с почечным синдромом, боливийская, аргентинская геморрагическая лихорадки, лихорадка Ласса, лихорадка Марбург и Эбола и др.), различаемых по этиологии, механизму возникновения и клиническим проявлениям.
Среди всех известных клинических форм наибольшее значение для нашей страны имеют геморрагическая лихорадка с почечным синдромом, омская и крымская геморрагические лихорадки.
ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА С ПОЧЕЧНЫМ СИНДРОМОМ
Геморрагическая лихорадка с почечным синдромом (А98.5) - ГЛПС (геморрагический нефрозонефрит, тульская, уральская, ярославская лихорадка) - острая инфекционная болезнь вирусной природы, характеризующаяся лихорадкой, интоксикацией, геморрагическим и почечным синдромами.
Этиология. Возбудитель болезни относится к семейству Bunyaviridae, включает 2 специфических вирусных агента (Хантаан и Пиумале), которые удается пассировать и накапливать в легких полевой мыши. Вирусы содержат РНК и имеют диаметр 80-120 нм, малоустойчивы - при температуре 50 °С сохраняются 10-20 мин.
Эпидемиология. ГЛПС - типичная зоонозная инфекция. Природные очаги заболевания находятся на Дальнем Востоке, в Забайкалье, Восточной Сибири, Казахстане и в европейской части страны. Резервуаром инфекции являются мышевидные грызуны: полевые и лесные мыши, крысы, полевки и др. От грызуна грызуну инфекцию передают гамазовые клещи и блохи. Мышевидные грызуны переносят инфекцию в латентной, реже в клинически выраженной форме, при этом они выделяют вирус во внешнюю среду с мочой и фекалиями. Человеку инфекция передается аспирационным путем - при вдыхании пыли со взвешенными инфицированными выделениями грызунов, контактным путем - при попадании инфицированного материала на царапины, порезы, скарификации или при втирании в неповрежденную кожу; алиментарным путем - при употреблении инфицированных выделениями грызунов пищевых продуктов (хлеб, овощи, фрукты и др.). Трансмиссивный путь передачи, считавшийся раньше ведущим, в настоящее время оспаривается. Непосредственная передача инфекции от человека человеку маловероятна.
ГЛПС встречается в виде спорадических случаев, но возможны локальные эпидемические вспышки.
Дети, особенно моложе 7 лет, болеют редко из-за ограниченного контакта с природой. Описаны вспышки ГЛПС в пионерских лагерях, детских садах, детских санаториях, расположенных близко к лесному массиву. Наибольшее число заболеваний регистрируется с мая по ноябрь. На Дальнем Востоке заболеваемость имеет подъемы: в мае-июле и особенно в октябре-декабре, что в целом совпадает с миграцией грызунов в жилые и хозяйственные помещения, а также с расширением контактов человека с природой и проведением сельскохозяйственных работ.
Патогенез. Инфекция первично локализуется в эндотелии сосудов и, возможно, в эпителиальных клетках ряда органов. После внутриклеточного накопления вируса наступает фаза вирусемии, что совпадает с началом болезни и появлением общетоксических симптомов. Вирусу ГЛПС свойственно капилляротоксическое действие. При этом происходит повреждение сосудистой стенки, нарушается свертываемость крови, что приводит к развитию тромбогеморрагического синдрома с возникновением множественных тромбов в различных органах, особенно в почках. В тяжелых случаях эти нарушения могут привести к кровоизлияниям во внутренние органы и большим полостным кровотечениям. Доказано токсическое действие вируса на ЦНС. В патогенезе ГЛПС также имеют значение аутоантигены, аутоантитела и циркулирующие иммунные комплексы.
Патоморфология. Морфологические изменения обнаруживаются преимущественно в почках. Почки резко увеличены, капсула напряжена, иногда имеются разрывы и множественные кровоизлияния. Корковый слой почки на разрезе желтовато-серого цвета, рисунок стерт, отмечаются небольшие кровоизлияния и некрозы. В мозговом веществе почек определяется выраженная серозная или серозно-геморрагическая апоплексия, нередко видны ишемические инфаркты, резкое перерождение эпителия прямых канальцев. Микроскопически в почках определяются полнокровие, очаговые отечно-деструктивные изменения сосудистых стенок, отек межуточной ткани, дистрофические изменения эпителия мочевых канальцев. Мочевые канальцы расширены, их просвет заполнен гиалиновыми и зернистыми цилиндрами, собирательные трубки сдавлены. В других внутренних органах (печень, поджелудочная железа, ЦНС, эндокринные железы, желудочно-кишечный тракт и др.) выявляются полнокровие, кровоизлияния, дистрофические изменения, зернистое перерождение, отек, стазы, рассеянные некрозы.
Клиническая картина. Инкубационный период продолжается от 10 до 45 дней, в среднем около 20 дней. Заболевание протекает циклично. Выделяют 4 стадии болезни: лихорадочную, олигурическую, полиурическую и реконвалесценции. Болезнь начинается, как правило, остро, с подъема температуры до 39 - 41 °С и появления общетоксических симптомов: тошноты, рвоты, вялости, заторможенности, расстройства сна, анорексии. С 1-го дня болезни отмечается сильная головная боль, преимущественно в лобной и височной областях, возможны также головокружения, познабливание, чувство жара, боли в мышцах конечностей, в коленных суставах, ломота во всем теле, болезненность при движении глазных яблок, сильные боли в животе, особенно в проекции почек. На 2-3-й день клинические симптомы достигают максимальной выраженности. Состояние ребенка часто тяжелое или очень тяжелое. Выражены симптомы интоксикации, гипертермия, тремор языка и пальцев рук, возможны галлюцинации, бред, судороги. Дети старшего возраста жалуются на «туман перед глазами», мелькание «мушек», снижение остроты зрения, видение предметов в красном цвете. При осмотре отмечаются одутловатость и гиперемия лица, пастозность век, инъекция сосудов конъюнктив и склер, сухость языка, гиперемия слизистых оболочек зева, больной ощущает боль в горле, жажду. В разгар заболевания нередко появляются геморрагическая энантема на слизистых оболочках мягкого неба и петехиальная сыпь на коже груди, в подмышечных впадинах, в области шеи, ключиц, располагающаяся в виде полос, напоминающих след от удара хлыста. Возможны также носовые, маточные и желудочные кровотечения. Могут появиться крупные кровоизлияния в склеру и в кожу, особенно в местах инъекций. Пульс в начале болезни учащен, но затем развивается брадикардия, при этом отмечается понижение артериального давления вплоть до коллапса или шока. Границы сердца не расширены, тоны приглушены, часто прослушивается систолический шум на верхушке. Иногда возникает клиническая картина очагового миокардита. Пальпация живота обычно болезненная в его верхней половине, у некоторых больных появляются симптомы раздражения брюшины. У половины больных увеличена печень, реже - селезенка. Стул чаще задержан, но возможны поносы с появлением крови в кале.
Олигурический период у детей наступает рано. Уже на 3-4-й, реже на 6-8-й день болезни снижается температура тела и резко падает диурез, усиливаются боли в пояснице. Состояние детей еще больше ухудшается в результате нарастания симптомов интоксикации и поражения почек. При исследовании мочи выявляются протеинурия, гематурия, цилиндрурия. Постоянно обнаруживаются почечный эпителий, нередко слизь и свертки фибрина. Всегда снижены клубочковая фильтрация и канальцевая реабсорбция, что приводит к олигурии, гипостенурии, гиперазотемии, метаболическому ацидозу. Снижается относительная плотность мочи. При нарастании азотемии возникает клиническая картина острой почечной недостаточности вплоть до развития уремической комы и эклампсии.
Полиурический период наступает с 8-12-го дня болезни и знаменует начало выздоровления. Состояние больных улучшается, постепенно стихают боли в пояснице, прекращается рвота, восстанавливаются сон и аппетит. Усиливается диурез, суточное количество мочи может достигать 3-5 л. Относительная плотность мочи снижается еще больше (стойкая гипоизостенурия).
Реконвалесцентный период продолжается до 3 - 6 мес. Выздоровление наступает медленно. Долго не проходит общая слабость, постепенно восстанавливаются диурез и относительная плотность мочи. Состояние постинфекционной астении может сохраняться в течение 6-12 мес.
В крови в начальном (лихорадочном) периоде отмечается кратковременная лейкопения, быстро сменяющаяся лейкоцитозом со сдвигом формулы влево до палочкоядерных и юных форм, вплоть до промиелоцитов, миелоцитов, метамиелоцитов. Можно выявить анэозинофилию, падение содержания тромбоцитов и появление плазматических клеток. СОЭ часто нормальна или повышена. При острой почечной недостаточности в крови резко возрастает уровень остаточного азота, уменьшается содержание хлоридов и натрия, но увеличивается количество калия.
Классификация. Наряду с типичными встречаются стертые и субклинические варианты болезни. В зависимости от выраженности геморрагического синдрома, интоксикации и нарушений функции почек различают легкие, среднетяжелые и тяжелые формы.
Течение. ГЛПС всегда протекает остро. При легких и среднетяжелых формах прогноз благоприятный. В тяжелых случаях может наступить летальный исход от кровоизлияния в головной мозг и кору надпочечников, геморрагического отека легких, надрыва коркового вещества почек, азотемической уремии, острой сердечно-сосудистой недостаточности.
Диагностика. ГЛПС диагностируют на основании характерной клинической картины: лихорадки, гиперемии лица и шеи, геморрагических высыпаний на плечевом поясе по типу следа от удара плетью, поражения почек, лейкоцитоза со сдвигом влево и появления плазматических клеток. Для диагностики имеют значение пребывание больного в эндемической зоне, наличие грызунов в жилище, употребление овощей, фруктов со следами погрызов. Специфические методы лабораторной диагностики включают ИФА, РИФ, реакцию гемолиза куриных эритроцитов и др.
ГЛПС дифференцируют с геморрагическими лихорадками другой этиологии, лептоспирозом, гриппом, сыпным тифом, острым нефритом, капилляротоксикозом, сепсисом и другими заболеваниями.
Лечение проводят в стационаре. Назначают постельный режим, полноценную диету с ограничением мясных блюд, но без уменьшения количества поваренной соли. На высоте интоксикации показаны внутривенные вливания 10% раствора глюкозы, раствора Рингера, альбумина, 5% раствора аскорбиновой кислоты. В тяжелых случаях назначают кортикостероиды из расчета 2-3 мг/ (кг. сут) преднизолона в 4 приема, курс составляет 5-7 дней. При сердечно-сосудистой недостаточности прописывают кордиамин, мезатон, при гипертензии - эуфиллин, папаверин. В олигурическом периоде вводят маннитол, полиглюкин, промывают желудок 2% раствором гидрокарбоната натрия. При нарастающей азотемии и анурии прибегают к экстракорпоральному гемодиализу с помощью аппарата «искусственная почка». При массивных кровотечениях назначают переливания крови и кровезаменителей. Для предупреждения тромбогеморрагического синдрома вводят гепарин. При угрозе бактериальных осложнений применяют антибиотики.
Профилактика направлена на уничтожение мышевидных грызунов на территории природных очагов, предупреждение загрязнения продуктов питания и водоисточников экскрементами грызунов, строгое соблюдение санитарно-противоэпидемического режима в жилых помещениях и вокруг них.
ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА
Омская геморрагическая лихорадка (А 98.1) - ОГЛ - острое инфекционное заболевание вирусной природы с трансмиссивным путем передачи, сопровождающееся лихорадкой, геморрагическим диатезом, скоропреходящим поражением почек, ЦНС и легких.
Этиология. Возбудитель болезни - вирус из рода Flavivirus, семейства Togaviridae. Содержит РНК, диаметр вириона 30-40 нм, патогенен для многих диких и лабораторных животных (ондатры, белых мышей, кроликов, морских свинок и др.), обнаруживается в крови больных в остром периоде болезни и в организме клещей Dermacentor pictus, являющихся главными переносчиками болезни.
Эпидемиология. Основным резервуаром инфекции являются ондатра и водяная крыса (водяная полевка), а также некоторые виды мелких млекопитающих и птиц. Доказаны длительное сохранение вируса в клещах и его способность передаваться потомству трансовариально. Человек заражается через укусы иксодовых клещей Dermacentor pictus. Возможно также заражение человека водным, пищевым, аспирационным и контактным путями. Наибольшее число заболеваний регистрируется в весеннелетние месяцы. От человека человеку инфекция не передается.
Патогенез. Основным патогенетическим звеном является поражение вирусом стенки сосудов, что обусловливает геморрагический синдром и очаговые кровоизлияния во внутренних органах. Важное значение имеет поражение вирусом центральной и вегетативной нервной системы, а также надпочечников и кроветворных органов. После перенесенного заболевания остается стойкий иммунитет.
Патоморфология. При ОГЛ отмечаются полнокровие и кровоизлияния во внутренние органы (почки, легкие, желудочно-кишечный тракт и др.). Микроскопически находят генерализованное поражение мелких кровеносных сосудов (капилляров и артериол) преимущественно в головном и спинном мозге, а также в легких.
Клиническая картина. Инкубационный период продолжается около 2-5 дней, но может удлиняться до 10 дней. Заболевание начинается остро, с подъема температуры тела до 39-40 °С, головной боли, озноба, ломоты во всем теле, тошноты, головокружения, болей в икроножных мышцах. Лицо больного гиперемировано, слегка одутловато, сосуды склер инъецированы, губы сухие, яркие, иногда покрыты кровянистыми корками. Постоянно обнаруживается гиперемия мягкого и твердого неба с пятнистой энантемой и геморрагическими точечными кровоизлияниями. Часто отмечается кровоточивость десен. С 1-2-го дня болезни появляется розеолезная и петехиальная сыпь на передней и боковой поверхностях груди, на разгибательных поверхностях рук и ног. В тяжелых случаях могут возникать обширные кровоизлияния в области живота, крестца и на голенях. В последующие дни на этих участках порой появляются обширные некрозы. Возможны также носовые, легочные, маточные и желудочно-кишечные кровотечения. Геморрагические симптомы обычно наблюдаются в первые 2-3 дня болезни, но возникают и в более поздние сроки - на 7-10-й день.
На высоте заболевания тоны сердца приглушены, отмечаются систолический шум на верхушке, брадикардия, расширение границ сердца влево, стойкая артериальная гипотония, иногда дикротия пульса, экстрасистолия. На ЭКГ имеются признаки диффузного поражения миокарда в результате нарушения коронарного кровообращения. В органах дыхания особенно часто отмечаются катаральные явления, а также очаговые, атипично протекающие пневмонии. Возможны явления менингоэнцефалита. Постоянно поражаются почки. Сначала появляется альбуминурия, затем присоединяются непродолжительная гематурия и цилиндрурия. В осадке мочи обнаруживают вакуолизированные зернистые клетки почечного эпителия. Диурез значительно снижен. С 1-го дня болезни в крови обнаруживаются лейкопения, умеренный нейтрофилез со сдвигом влево, тромбоцитопения; СОЭ нормальная или сниженная.
Различают легкие, среднетяжелые и тяжелые формы болезни. Встречаются стертые и субклинические формы.
Течение. В типичных случаях температурная реакция и симптомы интоксикации нарастают в течение 3-4 дней, в последующие дни состояние больного постепенно улучшается. Температура тела нормализуется на 5-10-й день болезни, полное выздоровление наступает через 1-2 мес и в более поздние сроки. У половины больных отмечаются повторные лихорадочные волны с возвратом основных симптомов болезни (обострения или рецидивы).
Диагностика. ОГЛ диагностируют на основании лихорадки, выраженного геморрагического диатеза в сочетании с катаральными явлениями, гиперемией лица и инъекцией сосудов склер, стойкой гипотонии и брадикардии. Диагностика облегчается при характерных изменениях в мочевом осадке и крови. Следует также учитывать пребывание в природном очаге инфекции. Из специфических методов используют выделение вируса и обнаружение нарастания титра специфических антител в РСК, РТГА, реакции диффузной преципитации (РДП) в агаровом геле или РН в динамике заболевания.
Дифференциальная диагностика. ОГЛ дифференцируют с лептоспирозом, клещевыми вирусными энцефалитами, гриппом, капилляротоксикозом, москитной лихорадкой, ГЛПС и другими геморрагическими лихорадками.
Лечение. Терапия исключительно патогенетическая, направлена на борьбу с интоксикацией (внутривенное введение 5-10% раствора глюкозы, реополиглюкина, плазмы и др.) и геморрагическими проявлениями (витамин К, викасол, гемотрансфузии и др.). В тяжелых случаях показаны кортикостероиды, сердечные средства, при бактериальных осложнениях назначают антибиотики.
Профилактика направлена на оздоровление природных очагов и предупреждение заражения детей в летних лагерях, детских садах, расположенных в зоне природного очага. Для активной иммунизации предложена убитая вакцина из мозга белых мышей, зараженных вирусом ОГЛ. Вакцинация проводится по строгим эпидемиологическим показаниям.
КРЫМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА
Крымская геморрагическая лихорадка (А98.0) - КГЛ - природноочаговая вирусная болезнь, передающаяся иксодовыми клещами. Заболевание сопровождается лихорадкой, тяжелой интоксикацией и геморрагическим синдромом.
Этиология. Возбудитель болезни - РНК-содержащий вирус из семейства Bunyaviridae, рода Nairovirus, диаметром 92-96 нм. Вирус можно выделить из крови больных в лихорадочном периоде, а также из взвеси растертых клещей - переносчиков болезни.
Эпидемиология. Резервуаром инфекции и переносчиком вируса является большая группа иксодовых клещей, у которых установлена трансовариальная передача вируса. Источником инфекции могут быть и млекопитающие (козы, коровы, зайцы и др.) со стертыми формами болезни или носительством вируса. Передача вируса человеку осуществляется при укусе иксодовых клещей. Возможно заражение человека при контакте с рвотными массами или кровью больных людей, а также с кровью больных животных. Весенне-летняя сезонность заболеваемости определяется активностью клещей-переносчиков.
Патогенез и морфологические изменения такие же, как и при ОГЛ и ГЛПС. Вирус поражает преимущественно эндотелий мелких сосудов почек, печени и ЦНС, что приводит к повышению проницаемости сосудистой стенки, нарушению системы свертывания крови по типу ДВС-синдрома и появлению геморрагического диатеза. Макроскопически находят множественные кровоизлияния во внутренние органы, а также в кожу и слизистые оболочки. Они укладываются в картину острого инфекционного васкулита с обширными дистрофическими изменениями и очагами некроза.
Клиническая картина. Инкубационный период длится от 2 до 14 дней, чаще 3-6 дней. Болезнь начинается остро или даже внезапно, с повышения температуры тела до 39-40 °С, озноба, сильной головной боли, общей слабости, разбитости, ломоты во всем теле, мышечных болей. Часто отмечаются боли в животе и пояснице, тошнота, рвота. Лицо больного, шея и слизистые оболочки зева гиперемированы, сосуды склер и конъюнктив инъецированы. Это так называемый начальный период болезни. Его длительность около 3-5 дней. Затем температура тела снижается, что совпадает с появлением геморрагического диатеза в виде петехиальных высыпаний на коже, слизистых оболочках полости рта, носовых кровотечений, гематом в местах инъекций. В особо тяжелых случаях могут быть маточные и желудочно-кишечные кровотечения.
При появлении геморрагического диатеза состояние больных утяжеляется. Дети становятся бледными, вялыми, адинамичными. Может появиться субиктеричность кожи и склер. Тоны сердца приглушены, отмечаются тахикардия, понижение артериального давления. Язык сухой, обложен беловато-серым налетом, иногда с геморрагическим пропитыванием. Печень умеренно увеличена. Симптом Пастернацкого положительный. Функция почек не нарушена, но в осадке мочи можно выявить альбуминурию и микрогематурию. С 1-го дня болезни в крови отмечаются лейкопения, нейтрофилез со сдвигом влево до палочкоядерных, эозинопения, тромбоцитопения; СОЭ нормальна или слегка повышена. При массивных кровотечениях развивается гипохромная анемия. Вторично возникают изменения в свертывающей и антисвертывающей системе крови.
Течение болезни часто бывает тяжелым, болезнь может закончиться смертью. У больных с благоприятным исходом геморрагические проявления исчезают довольно быстро - через 5-7 дней. Рецидивов и повторного геморрагического синдрома не бывает. Полное выздоровление наступает на 3-4-й нед болезни. У некоторых детей выздоровление может затягиваться из-за осложнений (пневмония, гепатаргия, почечная недостаточность, отек легких и др.).
Диагностика. КГЛ диагностируют на основании геморрагических проявлений на фоне общего токсикоза, изменений в крови и мочевом осадке. Имеет значение и эпидемиологический анамнез. Для лабораторного подтверждения используют методы выявления вируса и обнаружения нарастания титра специфических антител в динамике заболевания в РСК, РНГА и др.
КГЛ дифференцируют с гриппом, сыпным тифом, лептоспирозом, капилляротоксикозом, острым лейкозом, омской и другими геморрагическими лихорадками.
Лечение такое же, как при ГЛПС и ОГЛ.
Профилактика такая же, как и при ОГЛ и ГЛПС. Активная иммунизация не разработана.
ЖЕЛТАЯ ЛИХОРАДКА
Желтая лихорадка (А95) - ЖЛ - острое трансмиссивное инфекционное заболевание вирусной природы, с распространением в тропических регионах Африки и Южной Америки, характеризующееся геморрагическим синдромом, нефропатией и желтухой.
По МКБ-10 различают:
А95.0 - лесная желтая лихорадка;
А95.1 - городская желтая лихорадка;
А95.9 - желтая лихорадка неуточненная.
Этиология. Возбудителем является арбовирус группы В из семейства Togaviridae. К вирусу восприимчивы обезьяны, морские свинки, летучие мыши.
Эпидемиология. Основным резервуаром вируса ЖЛ являются больной человек и дикие животные (обезьяны, ежи, ленивцы, муравьеды и др.), переносчиками - комары. Восприимчивость к болезни всеобщая. Заболевания носят эпидемический характер. Заражение может произойти при попадании крови больного или умершего от ЖЛ человека на поврежденную кожу или слизистые оболочки. Инкубационный период составляет 3-6 дней.
Патогенез. Вирус ЖЛ проникает в регионарные лимфатические узлы, где происходит его размножение в течение всего инкубационного периода. Затем вирус попадает в кровь; вирусемия продолжается 3-4 дня. Распространяясь гематогенно, вирус проникает в печень, почки, костный мозг, селезенку. Как и при других геморрагических лихорадках, у больных ЖЛ развивается ДВС-синдром.
Патоморфология. Наибольшие изменения обнаруживаются в печени (некроз гепатоцитов с формированием телец Каунсильмена), а также в почках: они увеличены, желтоватого цвета, на разрезе отмечается жировая дистрофия. Можно выявить множественные кровоизлияния в легких, перикарде, желудочно-кишечном тракте, геморрагии и периваскулярные инфильтраты в головном мозге, дистрофические изменения в мышце сердца и других органах.
Классификация. Типичная форма ЖЛ имеет циклическое течение с 3 периодами (фазами): начальный, лихорадочный период - фаза гиперемии; период ослабления, падения температуры - фаза ремиссии; период венозного стаза. Клинические формы зависят от тяжести: легкая форма - транзиторная лихорадка, головная боль; среднетяжелая форма: лихорадка, головная боль, тошнота, носовые кровотечения, положительные сосудистые пробы, незначительная протеинурия, субклинический подъем билирубина, эпигастральные боли, боли в спине, головокружение, рвота, светобоязнь; тяжелая форма - выраженная лихорадка, сильная головная боль, боль в спине, интенсивная рвота, желтуха, олигурия; злокачественная форма - гипотермия, кровавая рвота, геморрагический синдром, желтуха, шок или коматозное состояние.
Клинические проявления. Заболевание начинается остро, с повышения температуры тела до 40-41 °С. Лицо становится красным, одутловатым, отмечается гиперемия шеи и верхней части груди, припухают губы, появляются головная боль, боли в мышцах, эпигастрии, тошнота, рвота с примесью крови, кровоточивость десен, выраженный геморрагический синдром, гипотония, желтуха, бред, нарушение сознания, коллапс, тяжелое поражение почек - анурия, протеинурия, цилиндрурия, желчные пигменты, азотемия. Летальный исход может наступить на 6-7-й день болезни от уремической или печеночной комы.
Специфическая диагностика: РСК, РН, РТГА, ИФА с раздельным определением специфических антител классов IgM и IgG.
Лечение. Методов специфической терапии ЖЛ нет. Симптоматическое лечение включает назначение антипиретиков, анальгетиков, противорвотных средств, борьбу с шоком, геморрагическим синдромом, использование противовирусного препарата - рибавирина, проведение инфузионной терапии.
Прогноз. Летальный исход (летальность около 5%) наступает на 6-7-й день, за 2-3 дня до смерти может развиться азотемическая или печеночная кома. При доброкачественном течении с 8-9-го дня болезни прекращаются рвота и кровотечения, повышается артериальное давление, снижается температура тела, увеличивается диурез.
Профилактика складывается из строгого эпидемиологического наблюдения на территории, где регистрируются случаи ЖЛ, плановой работы по истреблению комаров - переносчиков вируса, дезинсекции транспортных средств, прибывающих из мест, неблагополучных по ЖЛ, применения индивидуальных и коллективных средств защиты от комаров, карантинной изоляции не иммунизированных против ЖЛ лиц, прибывающих из мест, где есть случаи болезни, иммунизации населения против ЖЛ.
Вакцинопрофилактика. Вакцина против ЖЛ представляет собой ослабленный живой вирус штамма НД, выращенного на куриных эмбрионах. В 1 дозе вакцины (0,5 мл) содержится не менее 1000 ЛД 50 вируса, а также следовые количества белка куриного яйца и неомицина или полимиксина. Одну дозу вакцины вводят подкожно всем лицам старше 9 мес, выезжающим в эндемичные по ЖЛ страны. После вакцинации формируется напряженный иммунитет продолжительностью 10 лет и более. Вопрос о ревакцинации должен решаться индивидуально. Теоретически она показана только серонегативным лицам, но если обследование на специфические антитела невозможно, лучше ввести повторную дозу вакцины, особенно если интервал между вакцинациями более 10 лет. Вакцина против ЖЛ малореактогенна, но все же у части вакцинированных возможны умеренная лихорадка, недомогание и миалгии.
Противопоказания такие же, как и при введении других живых вакцин: иммунодефициты, беременность, иммунодепрессивная терапия, тяжелые аллергические реакции на яичный белок, неомицин или полимиксин.