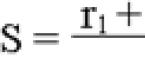Гиперинсулинизмом именуется клинический синдром, выражающийся завышением инсулиновых концентраций и понижением значений глюкозы в кровяном русле.
Следствием такого снижения поступления глюкозы в кровь является гипогликемия, которая ведет к слабости общего характера, увеличению чувства голода, головокружениям, психомоторной возбужденности и тремору.
При выявлении панкреатических образований применяется хирургическая тактика лечения, а в случае внепанкреатических вариантов выполняется лечение основной болезни и назначение определенного диетического питания.
Гипогликемическая болезнь, иначе – гиперинсулинизм – расстройство врожденного либо приобретенного характера, которое характеризуется возникновением относительной либо абсолютной гиперинсулинемии эндогенного типа.
Проявления заболевания были освещены в начале 20 века, врачом Харрисом и хирургом Оппелем.
Для справки!
Врожденный тип гиперинсулинизма встречается изредка, не более 1 ребенка из 50 000. Приобретенный тип возникает в 35-50 лет и в основном диагностируется у женщин.
Клиническая эндокринология нередко пользуется классификацией гиперинсулинизма в соответствии с причинами, спровоцировавшими патологию, и подразделяет заболевание на первичный и вторичный типы.
Первичный вариант подразделяется на такие типы:
Первичный тип гиперинсулинизма – последствие новообразования либо гиперплазии бета-клеток островковой части ПЖ.
Завышение инсулиновых значений в 90% способно возникать по причине доброкачественных опухолей, конкретно – инсулиномы, и изредка вследствие карцином, злокачественных опухолевых процессов.
Органический тип характеризуется тяжелым течением с яркими клиническими проявлениями и регулярными приступами гипогликемии.
Вторичная форма гиперинсулинизма подразделяется на такие типы:
Она имеет взаимосвязь с нехваткой контринсулярных физиологически активных соединений, а также может являться следствием нарушений функционирования печени и нервной системы.
Обострения возникают редко и фактически не имеют взаимосвязи с приемами пищи.
Для справки!
Суточное голодание при вторичном типе заболевания не приводит к обострению симптоматики и существенному падению глюкозы.
Медики выделяют 3 степени гиперинсулинизма:
- Легкая характеризуется отсутствием явной симптоматики в межприступном периоде, также нет и органического нарушения коры ГМ.
Обострения возникают не чаще, чем 1 раз/месяц и их легко ликвидировать.
- Средняя характеризуется большей частотой приступов, чем легкая стадия. Существует вероятность утери сознания и комы.
Межприступный период описывается небольшими поведенческими нарушениями.
- Тяжелая возникает в случае необратимых процессов коры ГМ. Приступы частые, завершаются утерей сознания.
В межприступном периоде человек дезориентирован, страдает от нарушений памяти, наблюдается тремор и эмоциональная нестабильность.
Основными причинными факторами, которые могут спровоцировать развитие врожденного типа гиперинсулинизма, выступают такие:
- внутриутробные нарушения развития;
- задержки роста внутриутробные;
- мутации генома.
Приобретенная панкреатическая форма является следствием образований зло- и доброкачественного характера ПЖ и гиперплазии ее бета-клеток.
Приобретенная непанкреатическая форма патологии развивается вследствие таких причин:
- нарушения пищевых привычек;
- разнообразные расстройства функционирования печени;
- злоупотребление сахаропонижающими медикаментами при СД;
- эндокринопатии, ведущие к понижению АКТГ, кортизола.
Существует вероятность, что гиперинсулинизм был спровоцирован нехваткой некоторых ферментов, принимающих участие в обмене глюкозы.
Механизмы развития и клиническая картина гиперинсулинизма
Глюкоза выступает ключевым питательным компонентом для ЦНС и требуется для верной работы ГМ.
Завышенные концентрации инсулина, скопление гликогена в печеночных структурах и замедленность гликогенолиза ведет к понижению значений глюкозы в кровяном русле.
Гипогликемия ведет к замедленности энергетических и обменных процессов в клеточных структурах мозга.
В это время выполняется активизация функции симпатоадреналовой системы, усиливается синтез кетахоламинов и прогрессирует гиперинсулинический приступ.
Продолжительная нехватка глюкозы ведет к расстройству всех метаболических процессов, повышение кровоснабжения ГМ и спазм сосудов периферии может стать основой для развития инфаркта.
Если в процесс были вовлечены средний, продолговатый мозг, а также варолиев мост прогрессируют судороги, происходят сбои деятельности сердца и дыхательной системы.
Симптоматическая картина гиперинсулинизма обуславливается падением показателей глюкозы в кровяном русле. Стартовая симптоматика состояния заключается в следующем:
- увеличение чувства голода;
- усиленное функционирование потовых желез;
- слабость общего характера;
- тахикардия.
В дальнейшем пациент ощущает такие негативные проявления гиперинсулинизма:
- ощущение беспричинного страха;
- тревожные состояния;
- тремор;
- излишняя вспыльчивость.

При прогрессировании приступа возникает ощущение дезориентации в пространстве, парестезии, вероятны судороги. В случае отсутствия медицинской помощи развивается гипогликемическая кома.
В межприступном периоде пациент испытывает следующее:
- ослабление способности к запоминанию;
- эмоциональная слабость;
- апатичные состояния;
- онемение тела, в частности – конечностей.
По причине частых приемов пищи с быстрыми углеводами стремительно растет вес и развивается ожирение.
При игнорировании состояния могут возникать такие нарушения здоровья, которые условно возможно подразделить на поздние и ранние.
Ранние последствия возникают в несколько часов после приступа и выражаются инсультом и инфарктом по причине стремительного падения интенсивности обменных процессов ГМ и сердца.
Поздние способны давать про себя знать по истечении месяцев и даже лет после приступа, они выражаются следующими состояниями:
- расстройства памяти;
- нарушения речи;
- энцефалопатия;
- паркинсонизм.
При несвоевременном диагностировании и отсутствии адекватной терапии происходит истощение эндокринных возможностей ПЖ и , синдром метаболический.
Диагностирование патологии
Диагностика базируется на симптоматических проявлениях, сведениях анамнеза болезни.
Врач определяет возможное присутствие генетических и прочих патологических процессов, а после производятся аппаратные и лабораторные исследования:
- Определение значений глюкозы в кровяном русле. Иначе – гликемический профиль пациента.
- При отклонениях гликемического профиля назначается проба с голоданием.
- Выполняются тесты на восприимчивость к лейцину и толбутамиду.
- По итогам теста на восприимчивость назначают прохождение УЗ-исследования брюшины и конкретно , МРТ ГМ, МРТ ПЖ, сцинтиграфия поджелудочной.
Дифференцирование требуется по отношению к синдрому Золлингера-Эллисона, СД 2 типа, неврологическим патологиям и психическим расстройствам.
Терапевтические меры
Терапевтические меры имеют зависимость от первопричины гиперинсулинемии.
В случае органического происхождения требуется оперативное вмешательство, выраженное частичной резекцией ПЖ либо же тотальной панкреатэктомией, энуклеацией образования.
Серьезность хирургического вмешательства выбирается в соответствии с объемами и локализацией опухолевого процесса.
После вмешательства нередко выявляется , которая нуждается в коррекции медикаментозными препаратами и диетического питания с заниженными углеводными концентрациями.

Значения приходят к норме приблизительно по истечении месяца с момента операции.
В случае неоперабельных образований выполняют паллиативное лечение, которое целенаправленно на предотвращение гипогликемии.
При злокачественных процессах в качестве вспомогательной меры выступает химиотерапия.
Терапия тяжелых вариантов гиперинсулинизма при условии пациента выполняется в реанимационном стационаре с выполнением дезинтоксикационного инфузионного лечения – вводятся В/В препараты адреналина и глюкокортикоиды.
Прогноз и профилактические меры
Прогноз в случае гиперинсулинизма зависит от этапа патологии и первопричин. Иссечение доброкачественных образований в 9 из 10 случаев ведет к выздоровлению.
При злокачественных либо неоперабельных новообразованиях, которые ведут к необратимым изменениям неврологического плана, требуется постоянный мониторинг показателей пациента.
Терапия первичной патологии при функциональном типе гиперинсулинизма ведет к регрессу симптоматики и излечении.
Профилактические меры подразумевают нормализацию питания и пересмотр пищевых привычек пациента – приемы пищи должны иметь периодичность в 2-3 часа, а также обязательно соблюдение питьевого режима.
- ограничение потребления ;
- отказ от табакокурения;
- мониторинг значений сахара в кровяном русле.
Для поддержания и коррекции , регулярно занимался умеренной физической активностью.
Многие заболевания, протекающие в хронической форме, часто предшествует возникновению сахарного диабета.
Например, гиперинсулинемия у детей и у взрослых людей выявляется в редких случаях, но указывает на чрезмерную выработку гормона, способного спровоцировать понижение уровня сахара, кислородное голодание и дисфункцию всех внутренних систем. Отсутствие лечебных мероприятий, направленных на подавление производства инсулина, может привести к развитию неконтролируемого диабета.
Причины патологии
Гиперинсулинизм в медицинской терминологии считается клиническим синдромом, возникновение которого происходит на фоне чрезмерного роста уровня инсулина.
В таком состоянии в организме наблюдается падение значения содержащейся в крови глюкозы. Недостаток сахара способен спровоцировать кислородное голодание мозга, следствием которого могут стать нарушения функционирования отделов нервной системы.

Гиперинсулизм в некоторых случаях протекает без особых клинических проявлений, но чаще всего заболевание приводит к тяжелой интоксикации.
Формы заболевания:
- Врожденный гиперинсулинизм . В его основе лежит генетическая предрасположенность. Заболевание развивается на фоне протекающих в поджелудочной железе патологических процессов, препятствующих нормальному продуцированию гормонов.
- Вторичный гиперинсулинизм . Эта форма прогрессирует вследствие других заболеваний, которые вызвали чрезмерную секрецию гормона. Функциональный гиперинсулинизм имеет проявления, сочетающиеся с нарушениями в углеводном обмене и выявленные при внезапном росте концентрации гликемии в кровотоке.
Основные факторы, способные вызвать рост уровня гормона:
- производство клетками непригодного инсулина с отличным от нормы составом, который не воспринимается организмом;
- нарушение резистентности, вследствие чего возникает неконтролируемая выработка гормона;
- отклонения в транспортировке глюкозы по кровотоку;
- избыточный вес;
- атеросклероз;
- наследственная предрасположенность;
- анорексия, имеющая нейрогенную природу и связанную с навязчивой мыслью о лишней массе тела;
- онкологические процессы в брюшной полости;
- несбалансированное и несвоевременное питание;
- злоупотребление сладостями, приводящее к росту гликемии, а, следовательно, и повышенной секреции гормона;
- патологии печени;
- бесконтрольная инсулинотерапия или чрезмерный прием препаратов для понижения концентрации глюкозы, что приводит к появлению медикаментозной ;
- эндокринные патологии;
- недостаточное количество ферментных веществ, принимающих участие в процессах обмена.
Причины гиперинсулинизма могут длительное время никак себя не проявлять, но при этом губительно сказываются на работе всего организма.
Группы риска
Развитию гиперинсулинемии чаще всего подвержены следующие группы людей:
- женщины, у которых выявлен поликистоз яичников;
- люди, имеющие генетическую наследственность к этому заболеванию;
- пациенты с нарушениями в работе нервной системы;
- женщины, находящиеся в преддверии менопаузы;
- пожилые люди;
- пациенты, ведущие малоактивный образ жизни;
- женщины и мужчины, получающие гормональную терапию или препараты из группы бета-блокаторов.

Симптомы гиперинсулинизма
Заболевание способствует резкому набору массы тела, поэтому большинство диет оказываются неэффективными. Жировые отложения у женщин образуются в зоне талии, а также брюшной полости. Это вызвано большим депо инсулина, хранящегося в форме специфического жира (триглицерида).
Проявления гиперинсулинизма во многом схожи с признаками, развивающимися на фоне гипогликемии. Начало приступа характеризуется повышением аппетита, слабостью, потливостью, тахикардией и ощущением голода.
Впоследствии присоединяется паническое состояние, при котором отмечается присутствие страха, тревоги, дрожи в конечностях и раздражительности. Затем возникают дезориентация на местности, онемение в конечностях, возможно появление судорог. Отсутствие лечения может привести к потере сознания и коме.
Степени болезни:
- Легкая. Она характеризуется отсутствием каких-либо признаков в периоды между приступами, но при этом продолжает органически поражать кору головного мозга. Пациент отмечает ухудшение состояния не менее 1 раза на протяжении календарного месяца. Для купирования приступа достаточно применить соответствующие лекарственные препараты или употребить сладкую пищу.
- Средняя. Частота возникновения приступов – несколько раз в месяц. Человек может потерять сознание в этот момент или впасть в кому.
- Тяжелая. Такая степень болезни сопровождается необратимыми поражениями головного мозга. Приступы часто возникают и практически всегда приводят к потере сознания.
Проявления гиперинсулизма практически не отличаются у детей и взрослых людей. Особенностью течения болезни у маленьких пациентов является развитие приступов на фоне более низких показателей гликемии, а также высокая частота их повторения. Результатом постоянных обострений и регулярного купирования такого состояния препаратами становится нарушение психического здоровья у детей.
Чем опасно заболевание?
Любая патология может привести к осложнениям, если своевременно не предпринимать никаких действий. Гиперинсулинемия не является исключением, поэтому также сопровождается опасными последствиями. Заболевание протекает в острой и хронической формах. Пассивное течение приводит к притуплению мозговой деятельности, негативно влияет на психосоматическое состояние.
Основные осложнения:
- нарушения в функционировании систем и внутренних органов;
- развитие диабета;
- ожирение;
- кома;
- отклонения в работе сердечно-сосудистой системы;
- энцефалопатия;
- паркинсонизм
Гиперинсулинемия, возникшая в детском возрасте, отрицательно сказывается на развитии ребенка.

Диагностика
Выявить болезнь часто бывает сложно из-за отсутствия специфических симптомов.
При обнаружении ухудшения самочувствия требуется консультация врача, который сможет определить источник такого состояния с помощью следующих диагностических исследований:
- анализ на гормоны, вырабатываемые гипофизом и поджелудочной железой;
- МРТ гипофиза, чтобы исключить онкологию;
- УЗИ брюшной полости;
- измерение давления;
- проверка уровня гликемии.
Постановка диагноза осуществляется на основе анализа полученных результатов обследования и жалоб пациента.
Лечение болезни
Терапия зависит от особенностей течения болезни, поэтому отличается в периоды обострения и ремиссии. Для купирования приступов требуется применение препаратов, а в остальное время достаточно соблюдать диету и проводить лечение основной патологии (диабета).
Помощь при обострении:
- съесть углевод или выпить сладкую воду, чай;
- струйно ввести раствор глюкозы, чтобы стабилизировать состояние (максимальное количество – 100 мл/1 раз);
- при наступлении комы нужно выполнить внутривенное введение глюкозы;
- при отсутствии улучшений следует сделать инъекцию адреналина или же глюкагона;
- применить транквилизаторы при судорогах.
Больные, находящиеся в тяжелом состоянии, должны быть доставлены в стационар и проходить лечение под наблюдением врачей. При органическом поражении железы может потребоваться резекция органа и проведение хирургического вмешательства.
Диета при гиперинсулинемии подбирается с учетом тяжести течения заболевания. Частые и сложно поддающиеся купированию приступы предусматривают присутствие повышенного количества углеводов в ежедневном рационе (до 450 г). Потребление жиров и белковой пищи при этом должно сохраняться в пределах нормы.
При нормальном течении болезни максимальное количество углеводов, поступивших с пищей за сутки, не должно превышать 150 г. Сладости, кондитерские изделия, алкоголь должны быть исключены из рациона.
Видео от эксперта:
Для сокращения проявлений гиперинсулинемии важно постоянно держать под контролем течение диабета и следовать основным рекомендациям:
- дробно и сбалансировано питаться;
- постоянно проверять уровень гликемии, корректировать ее при необходимости;
- соблюдать нужный питьевой режим;
- вести здоровый и активный образ жизни.
Если же чрезмерное производство инсулина стало следствием конкретного заболевания, то основная профилактика развития приступов сводится к лечению патологии, выступающей в роли основной причины их появления.
Врожденный гиперинсулинизм
М.А. МЕЛИКЯН Congenital hyperinsulinism
НИИ детской эндокринологии Эндокринологического научного центра, Москва
Врожденный гиперинсулинизм (ВГИ) - одна из основных причин развития персистирующих гипогликемических состояний в детском возрасте. Биохимически ВГИ характеризуется неадекватной гиперсекрецией инсулина в-клетками поджелудочной железы. ВГИ является гетерогенным заболеванием в отношении как клинических проявлений и морфологических форм, так и молекулярно-генетических дефектов, лежащих в его основе. В настоящей статье изложены современные взгляды на основные механизмы развития ВГИ, представлена клиническая характеристика заболевания, предложены международные протоколы обследования и лечения детей, страдающих данной патологией.
Ключевые слова: врожденный гиперинсулинизм, незидиобластоз, гипогликемический синдром, АТФ-зависимые калиевые каналы.
Congenital hyperinsulinism (CHI) is one of the main causes underlying the development of persistent hypoglycemic conditions in children. Biochemically, CHI is characterized by inadequate insulin secretion from pancreatic в-cells. CHI is a heterogeneous pathology in terms of clinical manifestations, morphological features, and molecular-genetic defects contributing to its development. The present paper is focused on the current views of CHI pathogenesis; the clinical characteristic of the disease is given and the internationally accepted protocols for the examination and treatment of children with congenital hyperinsulinism are described.
Key words: congenital hyperinsulinism, nesidioblastosis, hypoglycemic syndrome, ATP-dependent-potassium channels.
Врожденный гиперинсулинизм (ВГИ) - наследственное заболевание, характеризующееся неадекватной гиперсекрецией инсулина р-клетками поджелудочной железы, что приводит к развитию персистирующих гипогликемических состояний. В литературе описаны 8 генов, участвующих в развитии ВГИ. От 40 до 60% случаев ВГИ связаны с дефектами генов КСШ11 и АВСС8, кодирующих белки, которые участвуют в работе АТФ-зависимых калиевых каналов р-клеток поджелудочной железы. Около 15-20% связаны с активирующими мутациями в генах GCK и GLUD1, участвующих в регуляции внутриклеточного метаболизма глюкозы. В литературе также имеются единичные описания случаев ВГИ, связанных с дефектами генов HADH, НОТ4а, INSR, иСР2. В 30-40% всех случаев ВГИ не удается выявить молекулярно-генетических дефектов в указанных генах.
Распространенность ВГИ варьирует от 1:30 000 до 1:50 000 новорожденных, а в популяциях с высоким уровнем близкородственных браков достигает 1:2500 новорожденных .
ВГИ был впервые описан как «идиопатиче-ская гипогликемия детского возраста» ученым I. MacQuarrie в 1954 г. В дальнейшем ВГИ обозначали такими терминами, как, например, «лейцин-чувствительная гипогликемия», «синдром дисрегуляции р-клеток», «персистирующие гипе-ринсулинемические гипогликемии младенческого возраста». Длительное время для определения ВГИ
использовался термин «незидиобластоз» . Этот термин был введен Г. Лейдло еще в 1938 г.
Незидиобластоз - тотальная трансформация протокового эпителия поджелудочной железы в р-клетки, продуцирующие инсулин. К настоящему времени доказано, что подобная морфологическая картина является нормальной в младенческом возрасте и не служит причиной гиперинсулинизма .
Морфологически ВГИ разделяют на 3 основные формы: диффузную, при которой поражены все р-клетки поджелудочной железы, фокальную, если очаг поражения ограничен небольшим участком гиперплазированных клеток, содержащих крупные ядра, и атипичную .
Истинной причиной гиперсекреции инсулина при ВГИ является чаще всего неадекватная работа АТФ-зависимых К-каналов р-клеток поджелудочной железы, что обусловлено молекулярно-генети-ческими дефектами генов КСШ11 и АВСС8 .
Этиология и патогенез. Нормальная секреция инсулина р-клетками поджелудочной железы является следствием повышения уровня внутриклеточной АТФ. Увеличение соотношения АТФ/АДФ приводит к закрытию АТФ-зависимых К-каналов, последующей деполяризации мембраны, открытию вольтажзависимых кальциевых каналов и входа Са2+ в клетку, стимулирующего выброс инсулина. Достаточный подъем АТФ достигается последовательным каскадом реакций окисления глюкозы (рис. 1).
© М.А. Меликян,2010
e-mail: [email protected]
Рис. 1. Механизм секреции инсулина Р-клеткой поджелудочной железы.
При поступлении в клетку глюкоза фосфорилируется до активного метаболита глюкозо-6-фосфата. Данная реакция происходит при активации фермента глюкокиназы. Лейцин также служит одним из основных стимуляторов секреции инсулина. Он является специфичным активатором фермента глутаматдегидрогеназы, катализирующей реакцию превращения глутамата в а-кетоглутарат. Глюкоза и лейцин активируют внутриклеточный цикл Кребса, в результате которого синтезируется АТФ. Увеличение соотношения АТФ/АДФ ингибирует работу АТФ-зависимых калиевых каналов, что влечет за собой деполяризацию мембраны и открытие вольтажзависимых кальциевых каналов. Вход интерстициального Са2+ в клетку стимулирует выброс инсулина.
При снижении уровня глюкозы в крови ее внутриклеточный метаболизм тормозится, что изменяет (уменьшает) соотношение АТФ/ АДФ и приводит к открытию калиевых каналов и закрытию кальциевых каналов, тем самым блокируя секрецию инсулина.
Нарушения функции АТФ-зависимых К-кана-лов, а также дефекты регуляции внутриклеточного метаболизма глюкозы могут приводить к развитию гиперинсулинемических гипогликемических состояний. Наиболее частой причиной ВГИ являются инактивирующие мутации генов KCNJ11 и ABCC8 .
АТФ-зависимые калиевые каналы р-клеток представляют собой октамерные структуры, внутренние отделы которых представлены 4 субъединицами белка Kir6.2, кодируемого геном KCNJ11, а наружные - 4 субъединицами белка SUR1, кодируемого геном ABCC8. Данные каналы способны изменять степень поляризации мембраны клетки. Функциональная активность каналов регулируется уровнем внутриклеточных адениновых нуклеотидов. Инактивирующие мутации генов KCNJ11 и ABCC8 приводят к закрытию данных каналов, что влечет за собой избыточное поступление Са2+ в клетку и гиперсекрецию инсулина .
Описаны как аутосомно-рецессивные, так и аутосомно-доминантные мутации указанных генов. К настоящему моменту выявлено более 150 мутаций в гене ABCC8 и 25 мутаций в гене KCNJ11 .
ВГИ, связанный с рецессивными мутациями генов KCNJ11 и ABCC8, характеризуется тяжелым течением, ранним дебютом гипогликемии и, как правило, не поддается консервативной терапии.
Доминантно наследуемые формы протекают мягче, манифестируют позже и в большинстве случаев чувствительны к терапии диазоксидом .
Помимо нарушений работы АТФ-зависимых калиевых каналов р-клеток причинами развития ВГИ могут служить нарушения работы ферментов, участвующих во внутриклеточном метаболизме глюкозы. К ним относятся глюкокиназа, глутаматдеги-дрогеназа и 3-гидрокси-ацилКоА-дегидрогеназа.
Глюкокиназа - один из важных регуляторных факторов секреции инсулина. Данный фермент катализирует реакцию фосфорилирования глюкозы в ее активный метаболит - глюкозо-6-фосфат. Активирующие доминантные мутации гена GCK приводят к увеличению экспрессии фермента, что влечет за собой гиперсекрецию инсулина . Данная форма ВГИ характеризуется вариабельностью клинической картины. Описано бессимптомное течение. Некоторые мутации проявляют себя лишь гипогли-кемическими состояниями после приема пищи при сохранении нормального уровня глюкозы крови натощак. Существуют также описания тяжелых, резистентных к терапии, форм .
Митохондриальный фермент глутаматдеги-дрогеназа (кодируется геном ОЬиБ1) катализирует реакцию превращения глутамина в а-кетоглутарат и аммоний. Мутации гена ОЬиБ1 ослабляют чувствительность фермента к лейцину, который явля-
ется его специфичным ингибитором, что приводит к повышению активности фермента и избыточной продукции АТФ за счет активирующего влияния лейцина и аммония на реакции цикла Кребса . Отмечается повышение уровня аммиака крови. Эта форма ВГИ также носит название гипераммо-ниемийной лейцинчувствительной гипогликемии. Мутации в гене ОЬиБ1 наследуются по аутосомно-доминантному типу. Гипогликемические состояния при дефектах глутаматдегидрогеназы купируются низкопротеиновой диетой, хорошо поддаются терапии диазоксидом .
Другой редкой причиной рецессивно наследуемого ВГИ являются дефекты гена НАБН, кодирующего фермент 3-гидрокси-ацилКоА-дегидрогеназу. Данный фермент катализирует предпоследнюю реакцию в процессе р-окисления короткоцепочечных жирных кислот, в результате которой образуется 3-кето-ацилКоА. Инактивирующие мутации гена НАДНприводят к гиперпродукции инсулина и избыточному накоплению продуктов кетогенеза. Механизм гиперинсулинизма при этих мутациях остается неясным. Это единственная форма гиперинсулине-мической гипогликемии, протекающая с кетозом. Характерно повышение уровня 3-гидроксибутирил-карнитина в крови и 3-гидроксиглутарата в моче. Как правило, течение мягкое и отмечается хороший терапевтический эффект от диазоксида .
Фокальные формы ВГИ формируются в случае соматического снижения гомозиготности унаследованной от отца мутации в генах АВСС8 и КСЫЛ1 и специфической потери материнской аллели в регионе импринтинга на 11р 15. При этом происходит изменение экспрессии импринтинговых генов в регионе 11р 15.5: снижается экспрессия генов Н19 и Р57К1Р2, являющихся супрессорами опухолевого роста, и увеличивается экспрессия гена, кодирующего инсулиноподобный фактор роста 2-го типа (IGF2), являющийся мощным фактором пролиферации клеток. Подобное сочетание нарушений им-
принтинга с наследованием мутации в генах КСШ11 или АВСС8 приводят к развитию фокального адено-матоза ткани поджелудочной железы . Данные формы заболевания составляют около 40% всех случаев ВГИ . По своим клиническим проявлениям фокальный ВГИ не отличается от диффузного. При своевременной постановке молекулярно-генетического диагноза и визуализации образования возможно хирургическое лечение в виде селективной резекции фокуса, что приводит к полному выздоровлению . Основные генетические формы ВГИ представлены в табл. 1.
Клиническая картина. ВГИ, как правило, манифестирует в неонатальный период, однако возможен и более поздний дебют, вплоть до 3-летнего возраста. Чем раньше проявляется заболевание, тем тяжелее оно протекает . Гипогликемические состояния при ВГИ обычно носят тяжелый характер и быстро приводят к развитию судорог и потере сознания. Описаны и мягкие формы, протекающие почти бессимптомно, проявляющиеся лишь гиподинамией и сниженным аппетитом. В связи с избыточной продукцией инсулина еще во внутриутробном периоде дети с ВГИ, как правило, рождаются крупными. При рождении часто выявляется макросомия, кардиомиопатия, гепатомегалия . У матерей может отмечаться избыточная прибавка массы тела во время беременности. Для поддержания нормогликемии детям с ВГИ требуются крайне высокие дозы глюкозы. Потребность во внутривенной инфузии раствора глюкозы может достигать 20 мг/кг/мин .
Диагностика. Основными критериями диагноза ВГИ служит определение уровня инсулина в плазме (более 2,0 ед/л) в момент гипогликемии (глюкоза крови <2,4 ммоль/л у детей старше 1 года и <2,2 ммоль/л у детей до года) . Кроме того, критериями, подтверждающими диагноз ВГИ, являются гипокетотический характер гипогликемий (отсутствие кетоновых тел в моче, низкий уровень 3-ги-
Таблица 1. Формы врожденного гиперинсулинизма в зависимости от молекулярно-генетической причины
Ген Хромосомная Белок Тип наследования Фенотип
локализация
КСШ11 11р15.1 Юг6.2 Аутосомно-рецессивный Тяжелые гипогликемии, резистентные к терапии.
АВСС8 SUR1 Аутосомно-доминантный Наследование отцовской мутации с потерей гетерозиготности Дебют в первые дни жизни Гипогликемии средней степени тяжести. Возможен эффект от консервативной терапии Фокальные формы. Степень тяжести гипогликемии может варьировать
ОСК 7р15-13 Глюкокиназа Аутосомно-доминантный Клиника вариабельна. Может встречаться изолированная постпрандиальная гипогликемия
оьит 10а23.3 Глутаматдегидро-геназа Аутосомно-доминантный Мягкое течение. Повышен уровень аммиака крови. Хороший эффект от консервативной терапии и на фоне низкопротеиновой диеты
НАБН 4д22-26 3-Гидрокси- ацилКоА-дегидрогеназа Аутосомно-рецессивный Мягкое течение. Протекает с кетозом. Чувствительна к консервативной терапии
дроксибутирата в крови), выраженный гиперглике-мический ответ на введение глюкагона (повышение уровня глюкозы крови более чем на 1,7 ммоль/л), высокий или нормальный уровень С-пептида на фоне гипогликемии, потребность в высоких дозах глюкозы (> 8 мг/кг/мин), низкие уровни аминокислот (валина, лейцина) и нормальные - контринсу-лярных гормонов (соматотропный гормон, корти-зол, глюкагон) в крови . Стоит отметить, что у многих пациентов с ВГИ отсутствует выраженный подъем уровня кортизола и глюкагона в ответ на гипогликемию. Данное обстоятельство связано с незрелостью гормональной системы контррегуляции, а также с ее истощением, вызванным персистирую-щим гипогликемическими состояниями . Детям с поздним дебютом заболевания показано проведение УЗИ и мультиспиральной компьютерной томографии поджелудочной железы с целью исключения объемного образования (инсулиномы). Всем пациентам с диагнозом ВГИ рекомендовано проведение молекулярно-генетического исследования генов КСШ11 и АВСС8 . При наличии дефектов генов, характерных для фокальных форм, показано проведение позитронно-эмиссионной томографии с 18 -флюорин-л- 3,4-дигидроксифенилаланином (ПЭТ с 18-Ф-допой) .
Дифференциальная диагностика. ВГИ необходимо дифференцировать от других форм гипогликемии, таких как врожденные дефекты р-окисления жирных кислот; синдромальные формы гиперин-сулинизма (синдром Беквита-Видемана, синдром Сотоса, синдром Ашера и др.), от врожденных заболеваний гликозилирования и инсулинпродуцирую-щими опухолями поджелудочной железы, дефицита контринсулярных гормонов, гликогеновых болезней печени, дефектов кетогенеза и глюконеогенеза. Помимо этого, не стоит забывать про транзиторные формы неонатального гиперинсулинизма, связанные с диабетической фетопатией, задержкой внутриутробного развития и перинатальной асфиксией . Схемы дифференциальной диагностики основных форм гипогликемического синдрома представлены в табл. 2.
Лечение. Основной целью лечения ВГИ является поддержание стойкой нормогликемии (3,5-6,0 ммоль/л). Даже единичные эпизоды гипогликеми-ческих состояний в первые месяцы жизни могут быть чреваты тяжелыми неврологическими осложнениями. В связи с высокой потребностью в глюкозе пациентам с ВГИ рекомендована постановка центрального катетера, дающая возможность введения больших объемов концентрированного раствора.
Таблица 2. Дифференциальная диагностика основных форм гипогликемического синдрома у детей
Гипогликемические состояния
Заболевание
Кетотические
Некетотические
Идиопатическая кетотическая гипогликемия
Дефицит контринсулярных гормонов (врожденный гипопитуитаризм, изолированный дефицит СТГ, первичная/вторичная надпочечни-ковая недостаточность) Гликогенозы 0, I, III, VI, IX типов
Дефекты глюконеогенеза (дефицит фосфо-энилпируваткарбоксиназы, дефицит фруктозо-1-6-бисфосфатазы) Врожденный гиперинсулинизм
Инсулинпродуцирующие опухоли
Дефекты р-окисления жирных кислот
Синдром Бэквита-Видемана
Врожденные заболевания гликозилирования типов!а, Ь
Возраст старше года, низкая масса тела при рождении, гипогликемии на фоне длительного голодания, инфекций, физических нагрузок. Снижение аланина в крови Задержка роста, гипогликемии на фоне стресса, инфекций, гипертермии. Низкие показатели ИФР-1/кортизола. Отставание костного возраста
Увеличение размеров печени, повышение уровня лактата, АлАТ, АсАТ, отсутствие гипергликемической реакции на введение глюкагона
Повышение уровня лактата, триглицеридов, холестерина, мочевой кислоты. Адекватная реакция на глюкагон
Потребность в высоких дозах глюкозы, ранний возраст, ма-кросомия при рождении
Возраст старше 8 лет, УЗИ-/МСКТ-признаки объемного образования поджелудочной железы
Сопутствующие кардиомиопатии. Изменения соотношения аминокислот по данным ТМС
Транзиторные гипогликемии, макросомия при рождении, гемигиперплазия, пупочные грыжи, характерная борозда на мочках ушей, фетальные опухоли, повышение уровня
Характерные стигмы дисэмбриогенеза (инвертированные соски, микроцефалия, остеодисплазия), задержка физического развития, диарея, рвоты, повышение уровня АлАТ, АсАТ, протеинурия_
Примечание. СТГ - соматотропный гормон; МСКТ - мультиспиральная компьютерная томография; ИФР-1 - инсулинопо-добный фактор роста 1-го типа; АлАТ - аланинаминотрансфераза; АсАТ - аспартатаминотрансфераза; ТМС - тандемная масс-спектрометрия.
Рекомендовано дробное кормление обогащенными углеводами продуктами. Некоторым пациентам требуется постановка желудочного зонда для адекватного питания . Блок кетогенеза, вызванный гиперсекрецией инсулина, лишает детей с ВГИ альтернативных ресурсов энергии для головного мозга, что крайне быстро приводит к развитию судорог и в отсутствие адекватного лечения к формированию автономной эпилепсии. По последним международным рекомендациям , пациентам с ВГИ показано поддерживать уровень глюкозы в крови не ниже 3,8-4,0 ммоль/л. Среди лекарственных препаратов, применяемых для лечения гиперинсулинемических гипогликемических состояний, препаратом выбора является диазоксид . Диазоксид - агонист АТФ-зависимых К-каналов р-клеток поджелудочной железы. Механизм его действия заключается в активации работы самих каналов. Эффективность терапии варьирует в зависимости от молекулярно-генетических дефектов. Большинство пациентов с рецессивно наследуемыми мутациями генов ^ШП и ABCC8, а также некоторыми мутациями гена GCK, резистентны к данному лечению . Для потенцирования действия диазоксида в некоторых случаях возможно присоединение хлортиа-зида. Нифедипин, являясь блокатором кальциевых каналов, имеет супрессорный эффект на секрецию инсулина. Его эффективность в лечении ВГИ крайне низкая, существуют лишь единичные описания его успешной монотерапии . Соматостатин, являясь аналогом одноименного гормона, активирует специфичные рецепторы, расположенные в ткани поджелудочной железы, что подавляет секрецию инсулина. Данный препарат эффективен в сочетании с дробным режимом кормления. В редких случаях возможно использование пролонгированных
форм, когда инъекция выполняется 1 раз в месяц . Глюкагон применяется в острых ситуациях для купирования гипогликемии. Его длительное использование возможно лишь в виде постоянной подкожной инфузии. Высокие дозы глюкагона (>20 мкг/кг/ч) вызывают обратную реакцию - выброс инсулина . В табл. 3 приведены основные лекарственные препараты для лечения ВГИ.
Хирургическое лечение ВГИ. В случае резистентности к указанным методам лечения и сохранения гипогликемического состояния, пациентам с ВГИ рекомендовано хирургическое лечение . При диффузных формах проводится субтотальная па-креатэктомия, когда удаляется 95-98% ткани поджелудочной железы. Данная операция является крайне ивалидизирующей, так как в 40-50% случаев приводит к развитию инсулинзависимого сахарного диабета (ИЗСД) . Подобное хирургическое вмешательство показано лишь при тяжелых, резистентных ко всем видам консервативного лечения формах ВГИ. При фокальных формах выполняется селективная резекция фокуса, результатом которой является полное выздоровление . Для дифференциальной диагностики диффузных и фокальных форм используют скрининг на молекулярно-генетические дефекты генов ^ШП и ABCC8 . В случае генетической верификации фокального ВГИ, для визуализации образования, используется ПЭТ с 18^-допой . Использование других методов визуализации, таких как ультразвуковое исследование, магниторезонанс-ная томография, мультиспиральная компьютерная томография, ПЭТ с фторглюкозой, неинформативно при данной патологии . Ранее для локализации фокуса проводилась селективная кальцийстимулиро-ванная ангиография сосудов поджелудочной железы, однако, учитывая инвазивность данной процедуры,
Таблица 3. Препараты для лечения гипогликемических состояний при врожденном гиперинсулинизме
Препарат Способ, кратность приема Доза Механизм действия Побочные эффекты
Диазоксид Перорально 3-4 раза в сутки 5- -20 мг/кг/сут Агонист АТФ- Часто: гипертрихоз, за-
зависимых К-каналов держка жидкости.
Редко: гиперурикемия, эо-
зинофилия, лейкопения,
гипотония
Хлортиазид (приме- Перорально 2 раза в сутки 7- 10 мг/кг/сут Активирует работу Гипонатриемия, гипокали-
няется в комбинации АТФ-зависимых емия
с диазоксидом) К-каналов. Потенциру-
ет эффект диазоксида
Нифедипин Перорально 3 раза в сутки 0,25 -2,5 мг/кг/сут Блокатор кальциевых Гипотония (редко)
Глюкагон Методом постоянной подкож- 1- -20 мкг/кг/ч Активирует гликогено- Тошнота, рвота. Редко: па-
ной инфузии (в помах) лиз и глюконеогенез радоксальный подъем ин-
Соматостатин Подкожно 3-4 раза в сутки. 5- 25 мкг/кг/сут Активация рецепторов Анорексия, тошнота, рво-
Постоянная подкожная инфу- к соматостатину 5-го та, метеоризм, диарея, хо-
зия. типа; ингибирует по- лелитиаз, подавление се-
Внутривенная инфузия ступление Са2+ в клетку, креции СТГ, ТТГ, АКТГ,
снижает активность глюкагона, задержка роста,
ацетилхолинов тахифилаксия
Примечание. СТГ - соматотропный гормон; ТТГ - тиреотропный гормон; АКТГ - адренокортикотропный гормон.
Рис. 2. Протокол лечения и наблюдения за пациентами с ВГИ .
а также большую частоту осложнений, в настоящий момент, ее практически не используют в мире . Международный протокол ведения пациентов с ВГИ представлен на рис. 2.
Отдаленные наблюдения. У большинства пациентов с ВГИ, тяжесть течения и частота эпизодов гипогликемии резко снижаются с увеличением возраста. Описано множество случаев спонтанного выздоровления. В случае консервативного лечения в среднем к 3-4 годам жизни среднесуточная доза диазоксида снижается до минимальной терапевтической (5 мг/кг/сут). В литературе имеются данные, свидетельствующие о развитии с возрастом сахарного диабета у неоперированных пациентов с ВГИ . Среди детей, перенесших субтотальную панкреатэктомию, около 40% имеют ИЗСД, до 60% не нуждаются в инсулинотерапии, 2-5% требуют лечения диазоксидом для поддержания нормогли-кемии . По данным разных авторов , задержка психомоторного развития отмечается у 30-40% всех пациентов с ВГИ. В 15-20% случаев выявлено
формирование автономной эпилепсии, при которой требуется терапия противосудорожными препаратами. Степень тяжести неврологических осложнений напрямую зависит от возраста манифестации заболевания, а также от своевременности и адекватности проводимой терапии.
В данном обзоре литературы были рассмотрены основные молекулярно-генетические предпосылки развития ВГИ, представлены современные взгляды на наличие взаимосвязей генотипа и фенотипа. На основании международного опыта предложены современные протоколы диагностики, лечения и наблюдения за детьми, страдающими ВГИ. Своевременная постановка диагноза, выбор адекватного лечения и динамический контроль позволяют минимизировать неврологические осложнения ги-погликемических состояний. Несмотря на прорыв в понимании этиологии и патогенеза ВГИ, в 50% случаев молекулярно-генетический диагноз остается неясным, что требует дальнейших исследований в этой области.
ЛИТЕРАТУРА
1. James C., Kapoor R.R., Ismail D. et al. The genetic basis of congenital hyperinsulinism. J Med Genet 2009;46:289-299.
2. Otonkoski T., Ammala C., Huopio H. et al. A point mutation inactivating the sulfonylurea receptor causes the severe form of persistent hyperinsulinemic hypoglycemia of infancy in Finland. Diabetes 1999;48:408-415.
3. De Leon D.D., Stanley C.A. Mechanisms of disease: advances in diagnosis and treatment of hyperinsulinism in neonates. Nat Clin Pract Endocrinol Metab 2007;3:57-68.
4. McQuarrie I. Idiopathic spontaneously occurring hypoglycemia in infants: clinical significance of problem and treatment. AMA Am J Dis Child 1954;87:399-428.
5. Rahier J., Guiot Y., Sempoux C. Persistent hyperinsulinaemic hypo-glycaemia of infancy: a heterogeneous syndrome unrelated to nesidioblastosis. Arch Dis Child Fetal Neonatal Ed 2000;82:F108-F112.
6. Kapoor R.R., Flanagan S.E., James C. et al. Hyperinsulinaemic hypoglycaemia. Arch Dis Child 2009;94:450-457.
7. Kapoor R.R., James C., Hussain K. Advances in the diagnosis and management of hyperinsulinemic hypoglycemia. Nat Clin Pract Endocrinol Metab 2009;5:2:101-112.
8. Thomas P., Ye Y., Lightner E. Mutation of the pancreatic islet inward rectifier Kir6.2 also leads to familial persistent hyperinsulinemic hypoglycemia of infancy. Hum Mol Genet 1996;5:1809- 1812.
9. Thomas P.M., Cote G.J., Wohllk N. et al. Mutations in the sulfonylurea receptor gene in familial persistent hyperinsulinemic hypoglycemia of infancy. Science 1995;268:426-429.
10. Nestorowicz A., Inagaki N., Gonoi T. et al. A nonsense mutation in the inward rectifier potassium channel gene, Kir6.2, is associated with familial hyperinsulinism. Diabetes 1997;46:1743-1748.
11. Dunne M.J., Kane C., Shepherd R.M. et al. Familial persistent hyperinsulinemic hypoglycemia of infancy and mutations in the sulfonylurea receptor. N Engl J Med 1997;336:703-706.
12. Flanagan S.E., Clauin S., Bellanne-Chantelot C. et al. Update of mutations in the genes encoding the pancreatic beta-cell K(ATP) channel subunits Kir6.2 (KCNJ11) and sulfonylurea receptor 1 (ABCC8) in diabetes mellitus and hyperinsulinism. Hum Mutat 2009;30:170-180.
13. Pinney S.E., MacMullen C., Becker S. et al. Clinical characteristics and biochemical mechanisms of congenital hyperinsulinism associated with dominant KATP channel mutations. J Clin Inv 2008;118:2877-2886.
14. Zelent D., Najafi H., Odili S. et al. Glucokinase and glucose homeostasis: proven concepts and new ideas. Biochem Soc Trans 2005;33:306-310.
15. Christesen H.B., Brusgaard K., Beck Nielsen H., Brock Jacobsen B. Non-insulinoma persistent hyperinsulinaemic hypoglycaemia caused by an activating glucokinase mutation: hypoglycaemia un-awareness and attacks. Clin Endocrinol (Oxford) 2008;68:1011.
16. Fahien L.A., MacDonald M.J., Kmiotek E.H. et al. Regulation of insulin release by factors that also modify glutamate dehydroge-nase. J Biol Chem 1980;263:13610-13614.
17. Weinzimer S.A., Stanley C.A., Berry G.T. et al. A syndrome of congenital hyperinsulinism and hyperammonemia. J Pediat 1997;130:661-664.
18. Zammarchi E., Filippi L., Novembre E., Donati M.A. Biochemical evaluation of a patient with a familial form of leucine-sensitive
hypoglycemia and concomitant hyperammonemia. Metabolism 1996;45:957-960.
19. Clayton P. T., Eaton S, Aynsley-Green A. et al. Hyperinsulinism in short-chain L-3-hydroxyacyl-CoA dehydrogenase deficiency reveals the importance of beta-oxidation in insulin secretion. J Clin Inv 2001;108:457-465.
20. Hussain K, Clayton P.T., Krywawych S. et al. Hyperinsulinism of infancy associated with a novel splice site mutation in the S CHAD gene. J Pediat 2005;146:706-708.
21. Ryan F., Devaney D, Joyce C. et al. Hyperinsulinism: molecular aetiology of focal disease. Arch Dis Child 1998;79:445-447.
22. Damaj L, le Lorch M, Verkarre V. et al. Chromosome 11p15 Paternal Isodisomy in Focal Forms of Neonatal Hyperinsulinism. J Clin Endocrinol Metab 2008;93:4941-4947.
23. Palladino A.A., Bennett M.J., Stanley C.A. Hyperinsulinism in infancy and childhood: when an insulin level is not always enough. Ann Biol Clin (Paris) 2009;67:3:245-254.
24. Wolfsdorf J.I., Weinstein D.A. Hypoglycemia in Children, Pediatric. 5th Edition. Endocrinology 2007;1:291-327.
25. Hussain K., Hindmarsh P., Aynsley-Green A. Neonates with symptomatic hyperinsulinemic hypoglycemia generate inappropriately low serum cortisol counterregulatory hormonal responses. J Clin Endocrinol Metab 2003;88:9:4342-4347.
26. Hussain K, Adzick N.S., Stanley C.A. et al. The diagnosis of ectopic focal hyperinsulinism of infancy with [ 18 F]-dopa positron emission tomography. J Clin Endocrinol Metab 2006;91:2839- 2842.
27. Hussain K., Blankenstein O., De Lonlay P., Christesen H.T. Hyper-insulinaemic hypoglycaemia: biochemical basis and the importance of maintaining normoglycaemia during management. Arch Dis Child 2007;92:568-570.
28. Aynsley-Green A., Hussain K, Hall J. et al. Practical management of hyperinsulinism in infancy. Arch Dis Child Fetal Neonatal 2000;82:98-107.
29. Glaser B., Landau H, Smilovici A., Nesher R. Persistent hyperin-sulinaemic hypoglycaemia of infancy: long-term treatment with the somatostatin analogue Sandostatin. Clin Endocrinol (Oxford) 1989;31:71-80.
30. Moens K., Berger V., Ahn J.M. et al. Assessment of the role of interstitial glucagon in the acute glucose secretory responsiveness of in situ pancreatic beta-cells. Diabetes 2002;51:669-675.
31. Greene S.A., Aynsley-Green A., Soltesz G., Baum J.D. Management of secondary diabetes mellitus after pancreatectomy in infancy. Arch Dis Child 1984;59:356-359.
32. De Vroede M., Bax N.M., Brusgaard K. et al. Laparoscopic diagnosis and cure of hyperinsulinism in two cases of focal adenomatous hyperplasia in infancy. Pediatrics 2004;114:e520-e522.
33. Gussinyer M., Clemente M., Cebrián R. et al. Glucose intolerance and diabetes are observed in the long-term follow-up of nonpancreatectomized patients with persistent hyperinsulinemic hypoglycemia of infancy due to mutations in the ABCC8 gene. Diabetes Care 2008;31:6:1257-1259.
34. Mercimek-Mahmutoglu S., Rami B., Feucht M. et al. Long-term follow-up of patients with congenital hyperinsulinism in Austria. J Pediatr Endocrinol Metab 2008;21:6:523-532.
35. Mazor-Aronovitch K., Gillis D., LobelD. et al. Long-term neurode-velopmental outcome in conservatively treated congenital hyper-insulinism. Eur J Endocrinol 2007;157:4:491-497.
При отсутствии лечения болезнь перейдет в неконтролируемый диабет.
Причины возникновения
Возникновение гиперинсулинизма говорит о патологическом функционировании организма. Причины могут крыться глубоко внутри и долгие годы не давать о себе знать. Такое заболевание чаще встречается у женщин, это связано с частыми гормональными перестройками. Основные причины возникновения:
- Выработка непригодного инсулина поджелудочной железой, который отличается составом и не воспринимается организмом.
- Нарушение восприимчивости. Рецепторы не идентифицируют инсулин, что приводит к неконтролируемой выработке.
- Сбои транспортировки глюкозы в крови.
- Генетическая склонность.
- Ожирение.
- Атеросклероз.
- Нейрогенная анорексия - психологическое нарушение на фоне навязчивой мысли об избыточном весе, что влечет за собой отказ от еды, а впоследствии эндокринные нарушения, анемию, колебания сахара в крови.
- Онкология в брюшной полости.
Вернуться к оглавлению
Группы риска
Предрасположенность к повышению уровня инсулина с развитием гиперинсулинизма возникает:
Женщины с поликистозом яичников чаще подвержены такому состоянию.
- У людей с плохой наследственностью. Если среди родственников есть те, у кого диагностировано заболевание, то риск увеличивается в несколько раз. Ученые доказали, что присутствие антигенов HLA приводит к появлению гиперинсулинизма.
- При нарушениях функционирования центральной нервной системы, головной мозг дает неправильный сигнал, что ведет к переизбытку инсулина в организме.
- У женского пола в преддверии менопаузы.
- При ведении малоактивного образа жизни.
- В преклонном возрасте.
- У пациентов с поликистозом придатков.
- У людей, принимающих гормональные препараты, бета-блокаторы.
Вернуться к оглавлению
Симптомы гиперинсулинизма
Функциональный гиперинсулинизм приводит к резкому набору веса, при этом диеты зачастую неэффективны. У женщин жир откладывается в области талии и брюшной полости. Это связано с большим запасом инсулина, который сохраняется в виде специфического жира триглицерида.
Стоит отметить, что гиперинсулинизм имеет много общих симптомов с гипогликемией:
Чем опасен коварный недуг?
Каждая болезнь при отсутствии грамотного лечения приводит к осложнениям. Гиперинсулинизм может иметь не только острую форму, но и хроническую, противостоять которой в разы сложнее. Хроническое заболевание притупляет мозговую деятельность и сказывается на психосоматическом состоянии больного, а у мужчин ухудшается потенция, что чревато бесплодием. Врожденный гиперинсулинизм в 30% случаев приводит к кислородному голоданию головного мозга и влияет на полноценность развития ребенка. Есть перечень других факторов, на которые следует обратить внимание:
- Заболевание сказывается на функционировании всех органов и систем.
- Гиперинсулинизм может спровоцировать сахарный диабет.
- Наблюдается постоянная прибавка в весе с вытекающими последствиями.
- Повышается риск наступления гипогликемической комы.
- Развиваются проблемы с сердечно-сосудистой системой.
Вернуться к оглавлению
Диагностика заболевания
Выявление гиперинсулинизма усложняется отсутствием специфических симптомов, а часто - бессимптомностью. При ухудшении общего состояния следует немедленно обратиться к доктору. Потребуется открытый анализ на гормоны с полной картиной работы поджелудочной железы и гипофиза. При подозрениях проводится МРТ гипофиза с маркером, которое исключит вероятность онкологии. Для женщин диагностика основана на УЗИ брюшной полости, репродуктивных органов, так как болезнь связана с выработкой гормонов. Для подтверждения результата следует измерить артериальное давление и проверить уровень сахара в крови. Во внимание берутся жалобы пациента, которые могут подтвердить наличие недуга.
Лечение болезни
Если гиперинсулинизм был выявлен на начальной стадии, есть высокие шансы вылечить заболевание. Питание играет первостепенную роль, составленная диета соблюдается, четко следуя графику. Увеличивается физическая нагрузка, что позволяет разогнать метаболизм, избавиться от избыточного веса. Беременность усложняет лечение, а диета будет иной. Доктор включит витаминный комплекс, позволяющий растущему организму развиваться полноценно. При надобности добавляются:
- лекарственные препараты, направленные на снижение артериального давления;
- метаболические лекарства;
- биодобавки, подавляющие аппетит.
Вернуться к оглавлению
Гиперинсулинизм у детей: общие сведения
Гипогликемия у большинства детей с гиперинсулинизмом проявляется обычно в первые 18 мес. жизни, но иногда позднее. Гиперинсулинизм - самая частая причина постоянной гипогликемии в первые месяцы жизни. Дети с гиперинсулинизмом обычно рождаются крупными, что связано с анаболическим эффектом инсулина во внутриутробном периоде. Однако в таких случаях сахарный диабет у матери отсутствует. Концентрация инсулина на фоне гипогликемии оказывается несоразмерно высокой. При гипогликемии, не связанной с гиперинсулинизмом, концентрация инсулина в плазме должна быть меньше 5 мкЕД/мл, во всяком случае не выше 10 мкЕД/мл, но при гиперинсулинизме она обычно превышает эти показатели. Некоторые авторы предлагают более строгие критерии и считают патологическим уже уровень инсулина выше 2 мкЕД/мл на фоне гипогликемии. Отношение инсулин (мкЕД/мл)/глюкоза (мг%), как правило, превышает 0,4; содержание кетоновых тел и свободных жирных кислот в плазме снижено.
Гипогликемия у детей с макросомией может наблюдаться с первых дней жизни. Однако при меньшей степени гиперинсулинемии она проявляется лишь через несколько недель или месяцев, когда детей начинают кормить реже, особенно по ночам, и гиперинсулинемия препятствует мобилизации эндогенной глюкозы. Обычные симптомы - повышенный аппетит, требующий более частого кормления, фасцикуляции, дрожь и явные судороги. Гипогликемия развивается уже через 4-8 ч после кормления, т.е. быстрее, чем в других случаях (табл. 140.1 и табл. 140.2). Для ее купирования приходится вводить экзогенную глюкозу в больших дозах (нередко большемг/кг/мин). Кетонемия или ацидоз отсутствуют. Содержание С-пептида и проинсулина в сыворотке крови на фоне гипогликемии повышено, что отличает гиперинсулинизм от искусственной гипогликемии, вызванной введением экзогенного инсулина. Пробы с толбутамидом или лейцином у грудных детей необязательны; гипогликемия неизбежно возникает уже через несколько часов после кормления, и в пробе крови, взятой в это время, можно одновременно определить содержание глюкозы, инсулина, кетоновых тел и свободных жирных кислот. Введение глюкагона на фоне гипогликемии значительно повышает уровень глюкозы в крови (не менее, чем на 40 мг%). Это свидетельствует о сохранности механизмов гликогенолиза и о том, что мобилизации глюкозы препятствует именно инсулин (табл. 140.3-3 , табл. 140.4-4).
Диагностике гиперинсулинемии способствует определение концентрации ИФР-связывающего белка-1 . Инсулин резко подавляет его секрецию, и при гипогликемии, связанной с гиперинсулинизмом, его уровень оказывается низким. При спонтанной гипогликемии или гипогликемии голодания (с кетонемией) уровень инсулина снижается, содержание этого белка повышено.
Эндогенный гиперинсулинизм следует отличать от семейного гиперинсулинизма и несемейного гиперинсулинизма. У грудных детей, обусловленного диффузной гиперплазией бета-клеток, а также их очаговой гиперплазией и бета-клеточными аденомами. Только по уровню инсулина в плазме разграничить эти состояния невозможно. В их основе лежат различные генетические нарушения в эндокринной части поджелудочной железы, приводящие к автономной секреции инсулина. Спонтанная или спровоцированная голоданием гипогликемия в таких случаях не сопровождается снижением его уровня (табл. 140.3).
Современные клинические, биохимические и молекулярно-генетические подходы позволяют разделить врожденный гиперинсулинизм (ранее называвшийся незидиобластозом) на отдельные нозологические формы. Одна из форм врожденной хронической гиперинсулинемической гипогликемии наследуется как аутосомно-рецессивный признак и характеризуется тяжелым течением. В ее основе лежат мутации, нарушающие функцию К+-каналов в бета-клетках поджелудочной железы (рис. 140.1). В норме глюкоза поступает в бета-клетки с помощью независимого от инсулина транспортера GLUT-2 . Под действием глюкокиназы она фосфорилируется, превращаясь в глюкозо-6-фосфат, и далее окисляется с образованием АТФ. Повышение молярного отношения АТФ/АДФ закрывает АТФ- чувствительные К+-каналы клеточной мембраны. Эти каналы состоят из двух субъединиц: KlR6.2 (относящегося к семейству К+-каналов аномального выпрямления) и тесно связанного с ним регуляторного компонента - рецептора сульфанилмочевины (SUR) . В норме АТФ-чувствительные К+-каналы открыты, но при повышении внутриклеточной концентрации АТФ они закрываются и в клетках накапливается калий. Клеточная мембрана деполяризуется, открываются потенциалзависимые Са2+-каналы, и Поступающий в клетку кальций стимулирует экзоцитоз (секрецию) инсулина.
Ген SUR и ген KIR6.2 располагаются близко друг к другу на коротком плече хромосомы 11 (там же, где локализован ген инсулина). Мутации, инактивирующие ген SUR (или, реже, ген KIR6.2) препятствуют открытию К+-каналов. Когда они закрыты, клеточная мембрана остается деполяризованной, кальций непрерывно поступает в клетку, стимулируя постоянную секцию инсулина. Описана и более легкая доминантная форма таких дефектов. К закрытию К+-каналов (вследствие чрезмерной продукции АТФ) и, соответственно, к гиперинсулинизму приводит также активирующая мутация гена глюкокиназы. Напротив, инактивирующие мутации этого гена обусловливают недостаточную секрецию инсулина и лежат в основе юношеского инсулиннезависимого сахарного диабета (MODY) .
Гиперинсулинизм: причины возникновения, симптомы, лечение
Выработка инсулина в организме человека регулируется работой поджелудочной железы, за производства данного вещества отвечают островки Лангерганса. Чрезмерный выброс гормона в кровь, свидетельствует о развитии патологии под название гиперинсулинизм, при которой уровень сахара в крови резко понижается. Встречается заболевание гиперинсулинизм у детей и взрослых, переносится очень тяжело, долго лечится.
Формы заболевания
По характеру протекания отличают хроническую форму заболевания и острую. Хроническое течение патологии часто заканчивается апатией, снижением умственного восприятия, слабостью, комой. Работа всех органов, систем нарушается. Исходя из того, что послужило причиной возникновения патологии, отличают:
- панкреатический (первичный), органический гиперинсулинизм;
- внепанкреатический (вторичный), функциональный гиперинсулинизм.
Первичное развитие болезни провоцируется сбоями работы поджелудочной, развитием определенных патологий этого органа. В том время, как вторичный возникает как следствие хронических заболеваний любого органа. Заболевание может поражать небольшую область поджелудочной железы, иметь очаговый характер, или охватывать полностью зоны островков.
Диагностируя форму патологию, специалисты на протяжении суток отслеживают состояние пациента, берут на анализ кровь, мочу, определяют гликемию с сахарной нагрузкой, делают пробы на адреналин, инсулин. Кроме того, при органической форме патологии, внезапная выработка инсулина не регулируется и не компенсируется гипогликемическими механизмами. Происходит это потому, что нарушается работа нейроэндокринной системы, образуется недостаток глюкозы.
Любая форма заболевания очень опасна, требует незамедлительного вмешательства специалистов, скорое, правильное лечение. Без опытного врача и специальной диагностики поставить диагноз нельзя.
Причины возникновения
Возникнуть болезнь может абсолютно в любом возрасте, даже у новорожденных. Данный вид патологии опасный, панкреатический гиперинсулинизм возникает по ряду причин:
- болезни центральной нервной системы;
- поражение островков Лангерганса опухолью, злокачественного и доброкачественной происхождения;
- диффузная гиперплазия (опухоль) поджелудочной железы;
- развитие сахарного диабета;
- ожирение;
- нарушение обмена веществ;
- болезни эндокринного характера.
Вторичная форма заболевания провоцируется болезнями печени, пищеварительной системы, желчного пузыря. Происходит такое от недостатка сахара в крови, что присуще некоторым заболеваниям эндокринного характера, нарушенном обмене веществ, длительном голодании, тяжелом физическом труде. Наряду с тем, что все причины более ли менее понятны, медики делают акцент, на то, что почему на поджелудочной железе развивается онкология, до сих пор остается невыясненным. Неясно что приводит к общему поражению, к частичному.
Симптоматика
В зависимости от того почему проявляется гиперинсулинизм, симптомы могут отличаться. Кроме низкого содержания сахара в крови, медики выделяют:
- головную боль;
- постоянную усталость;
- слабость;
- сонливость;
- бледность;
- обще недомогание;
- постоянное чувство голода;
- дрожь конечностей;
- повышенное раздражение;
- обмороки;
- судороги;
- понижение давления;
- повышенную потливость;
- понижение температуры тела;
- учащенное сердцебиение;
- ощущение страха;
- депрессивные состояния;
- состояние дезориентации.
В зависимости от формы заболевания, например, при функциональном гиперинсулинизме, симптоматика может быть более расширенной. В каждом конкретном случае одни симптомы превосходят другие или проходят совместно. Гиперинсулинизм у детей, проявляется не так выраженно, но в любом случае заметен, требует диагностику и лечение, патология постепенно будет нарастать провоцируя более обширную симптоматику. Так, если запустить болезнь, то скоро симптомы будут настолько выражены, что возможно состояние клинической комы.
Врожденный гиперинсулинизм
Современная медицина все чаще употребляет термин врожденный гиперинсулинизм, встречается патология у новорожденных, грудных детей. Причины патологии остаются неизученными, поэтому врачи предполагают, что здесь сказывается плохая наследственность, генетический дефект. Данную форму называют еще идиопатический гиперинсулинизм, его симптомы также мало выражены.
Как оказать первую помощь
Находясь рядом с человеком у которого произошел резкий выброс большого количества инсулина в кровь, главное самому не паниковать. Чтобы облегчить состояние больному, снять первичную симптоматику приступа, нужно дать больному сладкую конфету, налить сладкого чая. При потере сознания срочно вколоть глюкозу.
После того, как состояние улучшится и явных признаков на повтор не будет, больного нужно сразу отвезти в больницу или вызвать специалистов на дом. Без внимания подобное явление оставлять нельзя, человек нуждается в лечении, возможно срочной госпитализации, это нужно понимать.
Лечение
Сразу после установки правильного диагноза, врач назначает медикаментозное лечение, однако это при самых легких формах патологии. Чаще всего процедура сводится к хирургическому вмешательству, опухоль удаляется или вместе с ней определенная часть поджелудочной. После назначаются восстанавливающие функциональность поджелудочной и других органов, медикаментозные препараты.
Если наблюдается функциональный гиперинсулинизм, то лечение изначально концентрируется на устранении провоцирующих патологий, снижению данной симптоматики.
Питание
При лечении патологии функциональной формы заболевания, учитывают серьезность заболевания, возможность осложнений на работе других органов, сложность лечения. Все это приводит к тому, что больным рекомендуют специальную диету, которую ни в коем случае нельзя нарушать. Питание при гиперинсулинизме должно быть строго сбалансированным, насыщенным сложными углеводами. Прием пищи растягивается до 5-6 раз в день.
Профилактика
Опытные специалисты говорят, что на сегодняшний день, меры профилактики возникновения и разрастания опухолевых клеток на поджелудочной железе, неизвестны. Однако советуют поддерживать свой организм в целом, не допуская возникновения провоцирующих патологий:
- активно двигаться;
- правильно питаться, не переедать;
- вести правильный образ жизни;
- не допускать психических травм;
- постоянных физических и эмоциональных перегрузок не допускать;
- не употреблять препараты, способствующие снижению сахара в крови, без соответствующих на то рекомендаций врача.
Если все-таки не удается избежать подобной патологии, особенно когда речь заходит о новорожденных, страдающих данным заболеванием нужно обращаться незамедлительно в больницу. Выполнять все требования и рекомендации специалистов, соглашаясь на предложенные методы лечения. Только так, лечение гиперинсулинизма будет эффективным и впредь можно будет избежать рецидивов. Нужно помнить, что по статистике 10% таких пациентов умирают, по причине несвоевременного обращения за профессиональной помощью, запущенности патологии, отказов при лечении.
Гиперинсулинемия у детей
ГИПЕРИНСУЛИНИЗМ (греч, hyper- + инсулин) - клинический синдром, проявляющийся симптомами гипогликемии различной степени выраженности, обусловленный усиленной секрецией инсулина. При повышенной резистентности к инсулину Г. может протекать без клин, проявлений гипогликемии (см.).
Этиология
Г. наблюдается при инсулинпродуцирующих опухолях, исходящих из бета-клеток панкреатических островков Лангерганса (см. Инсулома), спонтанной идиопатической гипогликемии у детей, в начальных стадиях сахарного диабета (в т. ч. при функциональных реактивных гипогликемиях), при ожирении, демпинг-синдроме, при ряде эндокринных заболеваний (акромегалия, тиреотоксикоз, болезнь Иценко - Кушинга) либо может возникнуть под действием различных алиментарных раздражителей.
Патогенез
Г. при функциональной реактивной гипогликемии нейрогенного происхождения возникает вследствие чрезмерной реакции бета-клеток панкреатических островков на нормальную углеводную нагрузку и развивается через 1,5 - 4 часа после приема пищи; увеличение содержания в крови иммунореактивного инсулина (гиперинсулинемия) наблюдается через 0,5-1 час, т. е. в те же сроки, что и у здоровых, но абсолютная величина его значительно больше, чем у здоровых. При пробе с нагрузкой глюкозой: уровень сахара в крови увеличивается в пределах нормальных величин, но через 11/2-4 часа развивается гипогликемия с последующим самостоятельным восстановлением нормального содержания сахара в крови.
Г. при начальных стадиях сахарного диабета (см. Диабет сахарный) связан с усилением секреций инсулина при нагрузках углеводами. При проведении этим больным пробы на толерантность к глюкозе отмечают поздний максимальный подъем иммунореактивного инсулина и последующую более длительную инсулинемию на более высоком по сравнению со здоровыми уровне. Содержание сахара в крови натощак нормально или несколько повышено, но после приема глюкозы остается повышенным в течение 2-2,5 час., а к третьему часу уменьшается до гипогликемического уровня.
При демпинг-синдроме у больных, перенесших резекцию желудка, развитие Г. связано с быстрым всасыванием глюкозы при поступлении ее в кишечник и в кровь. Адекватно этому повышается секреция инсулина, и через 1-2 часа после еды наступает гипогликемия.
Патогенез
Патогенез Г. при повышенной идиопатической чувствительности к лейцину, чаще наблюдающийся у детей, не ясен. Считают, что в ответ на прием лейцина (с пищей) начинает чрезмерно выделяться инсулин. Г. при спонтанной идиопатической гипогликемии у детей чаще связан с гипертрофией и гиперплазией бета-клеток панкреатических островков, что чаще сопутствует наследственным формам сахарного диабета.
Клиническая картина
Клиническая картина характеризуется гипогликемическими состояниями, проявляющимися слабостью, повышенным аппетитом и потливостью, тахикардией, раздражительностью, в тяжелых случаях - появлением судорог, диплопией, психическими нарушениями (неадекватное поведение, неправильная оценка окружающей обстановки и т. д.), потерей сознания.
Однако при формах Г., не связанных с инсулиномой, гипогликемические состояния не бывают тяжелыми и сопровождаются симптомами повышенной активности симпатической нервной системы.
Диагноз
При подозрении на Г. необходимо исследовать кровь на содержание сахара. Обязательны повторные исследования натощак, а также в период приступа гипогликемии. Функциональные реактивные гипогликемии развиваются преимущественно днем, после приема пищи с большим содержанием углеводов. Содержание сахара в крови редко снижается ниже 50 мг%, больные, как правило, не теряют сознания. Содержание иммунореактив-ного инсулина в крови натощак часто повышено.
Важное значение в диагностике Г. имеет проведение функциональной пробы с голоданием в течение 18- 24 час., считая от последнего вечернего приема пищи, и проба с назначением низкокалорийной диеты, богатой белками, но с резким ограничением углеводов и жиров, в течение 72 час. При проведении такой пробы больной получает 200 г мяса, 200 г творога, 30 г масла, 50 г хлеба, 500 г овощей (кроме картофеля и бобовых). Ежедневно исследуют кровь на содержание сахара натощак и в течение дня. У больных с Г. обычно содержание сахара в крови уменьшается до 50 мг% и ниже.
Пробы на толерантность к глюкозе и инсулину у больных Г. могут дать различные результаты, поэтому они не имеют диагностической ценности.
Проводят пробы на чувствительность к толбутамиду и лейцину. После внутривенного введения 1 г толбутамида или лейцина (200 мг на 1 кг веса тела, можно per os) в крови больных Г. обнаруживают увеличение иммунореактивного инсулина и уменьшение сахара.
Лечение
Лечение должно быть направлено на устранение и предупреждение гипогликемии. Рекомендуется частое питание с полноценным содержанием белка в пище и равномерным распределением углеводов в течение дня.
При Г., связанном с повышенной чувствительностью к лейцину, следует ограничивать потребление продуктов, содержащих лейцин (молочные продукты). Больным со спонтанными гипогликемиями рекомендуют частый прием пищи, а в тяжелых случаях назначают препараты глюкокортикоидов, иногда АКТГ, глюкагона, адреналина.
При доброкачественных опухолях поджелудочной железы больным производят неполную резекцию железы, при злокачественных опухолях - расширенную панкреатэктомию (см.).
Гиперинсулинизм у детей
Гиперинсулинизм у детей, как и у взрослых, проявляется гипогликемическими состояниями различной степени выраженности. Однако гипогликемические состояния у детей появляются при более низком содержании глюкозы в крови, чем у взрослых. При частых повторных гипогликемических состояниях у детей быстрее, чем у взрослых, нарушается психика (истинные нарушения вследствие тяжелых гипогликемий с необратимым течением и ложные, которые проходят под влиянием лечения).
Механизм развития функционального Г. у детей, рожденных женщинами, больными сахарным диабетом, не ясен. Полагают, что Г. плода является компенсаторной реакцией на гипергликемию матери; у 60-80% детей, рожденных женщинами, больными сахарным диабетом, обнаруживают Г. У таких детей отмечают гиперплазию клеток поджелудочной железы. После рождения уровень глюкозы быстро снижается, и через 1-2 часа у новорожденного может наблюдаться гипогликемическое состояние. Низкий уровень глюкозы и свободных жирных к-т в крови- следствие тормозящего действия инсулина на липолиз. У этих детей наблюдается избыточный вес, что связано с анаболическим действием инсулина. У женщин с сахарным диабетом, выявленным в период беременности, инсулиновая активность сыворотки крови повышена, у новорожденных от матерей, больных сахарным диабетом, инсулиновая реакция на введение глюкозы более выражена, чем у детей, рожденных здоровыми женщинами.
Патогномоничные симптомы Г. у новорожденных отсутствуют. Судороги, цианоз, остановка дыхания и состояние летаргии могут наблюдаться у детей при наличии внутричерепной травмы, сепсиса, легочносердечных заболеваний, гипокальциемии и других метаболических нарушений. Диагноз Г. устанавливают по содержанию в крови сахара (20 мг% и менее у ребенка с нормальным весом при рождении).
Г., возникающий под действием алиментарных раздражителей, необходимо дифференцировать с врожденной непереносимостью к фруктозе, при к-рой гипогликемия не связана с Г. Это редкое заболевание характерно для детского возраста и проявляется развитием тяжелых гипогликемических состояний и рвоты после приема продуктов, содержащих фруктозу. Оно обусловлено врожденной недостаточностью фруктозо-1-фосфат-альдолазы, приводящей к накоплению фруктозо-1-фос-фата в печени. Исключение из питания продуктов, содержащих фруктозу, устраняет гипогликемию. У детей с тяжелой формой эритробластоза также может развиться функциональный Г.; причина его не ясна. Г. развивается у детей, больных конституционально-экзогенным ожирением. Коэффициент инсулиносекреции у этих больных увеличен. Исследование иммунореактивного инсулина может до нек-рой степени характеризовать функциональное состояние инсулярного аппарата больного ребенка: чем более выражено ожирение, тем выше содержание иммунореактивного инсулина в крови.
У тучных детей, больных диабетом, на ранних стадиях его развития содержание инсулина в крови натощак выше, чем у здоровых детей и у детей с ожирением без диабета, иногда более чем в 3 раза.
Коэффициент инсулиносекреции у этих больных снижен по сравнению со здоровыми, что говорит об относительном Г.
Лечение Г. у детей зависит от его формы. При доброкачественных опухолях поджелудочной железы проводится неполная резекция, а при злокачественных - расширенная панкреатэктомия. При врожденной непереносимости к фруктозе - исключение из пищи продуктов, содержащих ее. При Г. у детей, связанных с другими заболеваниями,- лечение основного заболевания.
Библиография: Николаев О. В. и Вейнбeрг Э. Г. Инсулома, М., 1968, библиогр.; Руководство по эндокринологии, под ред. Б. В. Алешина и др., М., 1973; Hardy J. D. Islet cell tumors, Amer. J. med. Sci., v. 246, p. 218, 1963; Howard J. М., Moss N. H. a. Rhoads J. E. Collective review, hyperinsulinism and islet cell tumors of pancreas with 398 recorded tumors, Int. Abstr. Surg., v. 90, p. 417, 1950; Koutras P. a. White R. R. Insulin-secreting tumors of the pancreas, Surg. Clin. N. Amer., v. 52, p. 299, 1972; Labhart A. Klinik der inneren Sekretion, B. u. a., 1971; RosenbloomA. L. a. Sherman L. The natural history of idiopathic hypoglycemia of infancy and its relation to diabetes mellitus, New Engl. J. Med., v. 274, p. 815, 1966; Textbook of endocrinology, ed. by R. H. Williams, Philadelphia, 1974.
Гиперинсулинизм
Гиперинсулинизм - клинический синдром, характеризующийся повышением уровня инсулина и снижением сахара в крови. Гипогликемия приводит к слабости, головокружению, повышению аппетита, тремору, психомоторному возбуждению. При отсутствии своевременного лечения развивается гипогликемическая кома. Диагностика причин состояния основывается на особенностях клинической картины, данных функциональных проб, динамическом исследовании глюкозы, ультразвуковом или томографическом сканировании поджелудочной железы. Лечение панкреатических новообразований – хирургическое. При внепанкреатическом варианте синдрома проводят терапию основного заболевания, назначают специальную диету.
Гиперинсулинизм
Гиперинсулинизм (гипогликемическая болезнь) - врожденное или приобретенное патологическое состояние, при котором развивается абсолютная или относительная эндогенная гиперинсулинемия. Признаки болезни впервые были описаны в начале ХХ века американским врачом Харрисом и отечественным хирургом Оппелем. Врожденный гиперинсулинизм встречается достаточно редко - 1 случай на 50 тыс. новорожденных. Приобретенная форма заболевания развивается в возрастелет и чаще поражает лиц женского пола. Гипогликемическая болезнь протекает с периодами отсутствия выраженной симптоматики (ремиссия) и с периодами развернутой клинической картины (приступы гипогликемии).
Причины гиперинсулинизма
Врожденная патология возникает вследствие внутриутробных аномалий развития, задержки роста плода, мутаций в геноме. Причины возникновения приобретенной гипогликемической болезни разделяют на панкреатические, приводящие к развитию абсолютной гиперинсулинемии, и непанкреатические, вызывающие относительное повышение уровня инсулина. Панкреатическая форма болезни встречается при злокачественных или доброкачественных новообразованиях, а также гиперплазии бета-клеток поджелудочной железы. Непанкреатическая форма развивается при следующих состояниях:
- Нарушения в режиме питания. Длительное голодание, повышенная потеря жидкости и глюкозы (поносы, рвота, период лактации), интенсивные физические нагрузки без потребления углеводной пищи вызывают резкое снижение уровня сахара в крови. Чрезмерное употребление в пищу рафинированных углеводов увеличивает уровень сахара крови, что стимулирует активную выработку инсулина.
- Поражение печени различной этиологии (рак, жировой гепатоз, цирроз) приводит к снижению уровня гликогена, нарушению обменных процессов и возникновению гипогликемии.
- Бесконтрольный прием сахароснижающих препаратов при сахарном диабете (производных инсулина, сульфанилмочевины) вызывает медикаментозную гипогликемию.
- Эндокринные заболевания, приводящие к снижению уровня контринсулиновых гормонов (АКТГ, кортизол): гипофизарный нанизм, микседема, болезнь Аддисона.
- Недостаток ферментов, участвующих в процессах обмена глюкозы (печеночная фосфорилаза, почечная инсулиназа, глюкозо-6-фосфатаза) вызывает относительный гиперинсулинизм.
Патогенез
Глюкоза является главным питательным субстратом центральной нервной системы и необходима для нормального функционирования головного мозга. Повышенный уровень инсулина, накопление гликогена в печени и торможение гликогенолиза приводит к снижению уровня глюкозы в крови. Гипогликемия вызывает торможение метаболических и энергетических процессов в клетках головного мозга. Происходит стимуляция симпатоадреналовой системы, увеличивается выработка катехоламинов, развивается приступ гиперинсулинизма (тахикардия, раздражительность, чувство страха). Нарушение окислительно-восстановительных процессов в организме приводит к снижению потребления кислорода клетками коры головного мозга и развитию гипоксии (сонливость, заторможенность, апатия). Дальнейший дефицит глюкозы вызывает нарушение всех обменных процессов в организме, увеличение притока крови к мозговым структурам и спазм периферических сосудов, что может привести к инфаркту. При вовлечении в патологический процесс древних структур мозга (продолговатый и средний мозг, варолиев мост) развиваются судорожные состояния, диплопия, а также нарушение дыхательной и сердечной деятельности.
Классификация
В клинической эндокринологии наиболее часто используется классификация гиперинсулинемии в зависимости от причин возникновения заболевания:
- Первичный гиперинсулинизм (панкреатический, органический, абсолютный) является следствием опухолевого процесса или гиперплазии бета-клеток островкового аппарата поджелудочной железы. Повышению уровня инсулина в 90% способствуют доброкачественные новообразования (инсулинома), реже – злокачественные (карцинома). Органическая гиперинсулинемия протекает в тяжелой форме с выраженной клинической картиной и частыми приступами гипогликемии. Резкое понижение уровня сахара в крови возникает утром, связано с пропуском приема пищи. Для данной формы заболевания характерна триада Уиппла: симптомы гипогликемии, резкое снижение сахара в крови и купирование приступов введением глюкозы.
- Вторичный гиперинсулинизм (функциональный, относительный, внепанкреатический) связан с дефицитом контринсулярных гормонов, поражением нервной системы и печени. Приступ гипогликемии возникает по внешним причинам: голодание, передозировка гипогликемических препаратов, интенсивная физическая нагрузка, психоэмоциональное потрясение. Обострения болезни возникают нерегулярно, практически не связаны с приемом пищи. Суточное голодание не вызывает развернутой симптоматики.
Симптомы гиперинсулинизма
Клиническая картина гипогликемической болезни обусловлена понижением уровня глюкозы в крови. Развитие приступа начинается с повышения аппетита, потливости, слабости, тахикардии и ощущения голода. Позже присоединяются панические состояния: чувство страха, тревога, раздражительность, дрожь в конечностях. При дальнейшем развитии приступа отмечается дезориентация в пространстве, диплопия, парестезии (онемение, покалывание) в конечностях, вплоть до возникновения судорог. При отсутствии лечения наступает потеря сознания и гипогликемическая кома. Межприступный период проявляется снижением памяти, эмоциональной лабильностью, апатией, нарушением чувствительности и онемением в конечностях. Частый прием пищи, богатой легкоусвояемыми углеводами, провоцирует увеличение массы тела и развитие ожирения.
В современной практике выделяют 3 степени гиперинсулинизма в зависимости от тяжести течения болезни: легкую, среднюю и тяжелую. Легкая степень проявляется отсутствием симптоматики межприступного периода и органического поражения коры головного мозга. Обострения болезни проявляются реже 1 раза в месяц и быстро купируются медикаментозными препаратами или сладкой пищей. При средней степени тяжести приступы возникают чаще 1 раза в месяц, возможна потеря сознания и развитие коматозного состояния. Межприступный период характеризуется легкими нарушениями поведенческого характера (забывчивость, снижение мышления). Тяжелая степень развивается при необратимых изменениях коры головного мозга. При этом приступы случаются часто и заканчиваются потерей сознания. В межприступном периоде пациент дезориентирован, память резко снижена, отмечается тремор конечностей, характерна резкая смена настроения и повышенная раздражительность.
Осложнения гиперинсулинизма
Осложнения можно условно разделить на ранние и поздние. К ранним осложнениям, возникающим в ближайшие часы после приступа, относят инсульт, инфаркт миокарда вследствие резкого снижения метаболизма сердечной мышцы и головного мозга. В тяжелых ситуациях развивается гипогликемическая кома. Поздние осложнения проявляются спустя несколько месяцев или лет от начала болезни и характеризуются нарушением памяти и речи, паркинсонизмом, энцефалопатией. Отсутствие своевременного диагностики и лечения заболевания приводит к истощению эндокринной функции поджелудочной железы и развитию сахарного диабета, метаболического синдрома, ожирения. Врожденный гиперинсулинизм в 30% случаев приводит к хронической гипоксии головного мозга и снижению полноценного умственного развития ребенка.
Диагностика гиперинсулинизма
Диагностика основывается на клинической картине (потеря сознания, тремор, психомоторное возбуждение), данных анамнеза заболевания (время начала приступа, его связь с приемом пищи). Эндокринолог уточняет наличие сопутствующих и наследственных заболеваний (жировой гепатоз, сахарный диабет, синдром Иценко-Кушинга), после чего назначает лабораторные и инструментальные исследования. Пациенту проводится суточное измерение уровня глюкозы крови (гликемический профиль). При выявлении отклонений выполняют функциональные пробы. Проба с голоданием используется для дифференциальной диагностики первичного и вторичного гиперинсулинизма. Во время теста измеряют С-пептид, иммунореактивный инсулин (ИРИ) и глюкозу в крови. Повышение данных показателей свидетельствует об органическом характере болезни.
Для подтверждения панкреатической этиологии заболевания проводят тесты на чувствительность к толбутамиду и лейцину. При положительных результатах функциональных проб показано УЗИ, сцинтиграфия и МРТ поджелудочной железы. При вторичном гиперинсулинизме для исключения новообразований других органов выполняют УЗИ брюшной полости, МРТ головного мозга. Дифференциальная диагностика гипогликемической болезни проводится с синдромом Золлингера-Эллисона, началом развития сахарного диабета 2 типа, неврологическими (эпилепсия, новообразования головного мозга) и психическими (неврозоподобные состояния, психоз) заболеваниями.
Лечение гиперинсулинизма
Тактика лечения зависит от причины возникновения гиперинсулинемии. При органическом генезе показано хирургическое лечение: частичная резекция поджелудочной железы или тотальная панкреатэктомия, энуклеация новообразования. Объем оперативного вмешательства определяется местоположением и размерами опухоли. После операции обычно отмечается транзиторная гипергликемия, требующая медикаментозной коррекции и диеты с пониженным содержанием углеводов. Нормализация показателей наступает через месяц после вмешательства. При неоперабельных опухолях проводят паллиативную терапию, направленную на профилактику гипогликемии. При злокачественных новообразованиях дополнительно показана химиотерапия.
Функциональный гиперинсулинизм в первую очередь требует лечения основного заболевания, вызвавшего повышенную продукцию инсулина. Всем больным назначается сбалансированная диета с умеренным снижением потребления углеводов (гр. в сутки). Отдается предпочтение сложным углеводам (ржаные хлебцы, макароны из твердых сортов пшеницы, цельнозерновые крупы, орехи). Питание должно быть дробным, 5-6 раз в день. В связи с тем, что периодические приступы вызывают у пациентов развитие панических состояний, рекомендована консультация психолога. При развитии гипогликемического приступа показано употребление легкоусвояемых углеводов (сладкий чай, конфета, белый хлеб). При отсутствии сознания необходимо внутривенное введение 40 % раствора глюкозы. При судорогах и выраженном психомоторном возбуждении показаны инъекции транквилизаторов и седативных препаратов. Лечение тяжелых приступов гиперинсулинизма с развитием комы осуществляют в условиях реанимационного отделения с проведением дезинтоксикационной инфузионной терапии, введением глюкокортикоидов и адреналина.
Прогноз и профилактика
Профилактика гипогликемической болезни включает в себя сбалансированное питание с интервалом в 2-3 часа, употребление достаточного количества питьевой воды, отказ от вредных привычек, а также контроль уровня глюкозы. Для поддержания и улучшения обменных процессов в организме рекомендованы умеренные физические нагрузки с соблюдением режима питания. Прогноз при гиперинсулинизме зависит от стадии заболевания и причин, вызывавших инсулинемию. Удаление доброкачественных новообразований в 90% случаев обеспечивают выздоровление. Неоперабельные и злокачественные опухоли вызывают необратимые неврологические изменения и требуют постоянного контроля за состоянием пациента. Лечение основного заболевания при функциональном характере гиперинсулинемии приводит к регрессии симптомов и последующему выздоровлению.
Что такое гиперинсулинемия и чем она опасна?
Многие заболевания, протекающие в хронической форме, часто предшествует возникновению сахарного диабета.
Например, гиперинсулинемия у детей и у взрослых людей выявляется в редких случаях, но указывает на чрезмерную выработку гормона, способного спровоцировать понижение уровня сахара, кислородное голодание и дисфункцию всех внутренних систем. Отсутствие лечебных мероприятий, направленных на подавление производства инсулина, может привести к развитию неконтролируемого диабета.
Причины патологии
Гиперинсулинизм в медицинской терминологии считается клиническим синдромом, возникновение которого происходит на фоне чрезмерного роста уровня инсулина.
В таком состоянии в организме наблюдается падение значения содержащейся в крови глюкозы. Недостаток сахара способен спровоцировать кислородное голодание мозга, следствием которого могут стать нарушения функционирования отделов нервной системы.
Гиперинсулизм в некоторых случаях протекает без особых клинических проявлений, но чаще всего заболевание приводит к тяжелой интоксикации.
- Врожденный гиперинсулинизм. В его основе лежит генетическая предрасположенность. Заболевание развивается на фоне протекающих в поджелудочной железе патологических процессов, препятствующих нормальному продуцированию гормонов.
- Вторичный гиперинсулинизм. Эта форма прогрессирует вследствие других заболеваний, которые вызвали чрезмерную секрецию гормона. Функциональный гиперинсулинизм имеет проявления, сочетающиеся с нарушениями в углеводном обмене и выявленные при внезапном росте концентрации гликемии в кровотоке.
Основные факторы, способные вызвать рост уровня гормона:
- производство клетками поджелудочной железы непригодного инсулина с отличным от нормы составом, который не воспринимается организмом;
- нарушение резистентности, вследствие чего возникает неконтролируемая выработка гормона;
- отклонения в транспортировке глюкозы по кровотоку;
- избыточный вес;
- атеросклероз;
- наследственная предрасположенность;
- анорексия, имеющая нейрогенную природу и связанную с навязчивой мыслью о лишней массе тела;
- онкологические процессы в брюшной полости;
- несбалансированное и несвоевременное питание;
- злоупотребление сладостями, приводящее к росту гликемии, а, следовательно, и повышенной секреции гормона;
- патологии печени;
- бесконтрольная инсулинотерапия или чрезмерный прием препаратов для понижения концентрации глюкозы, что приводит к появлению медикаментозной гипогликемии;
- эндокринные патологии;
- недостаточное количество ферментных веществ, принимающих участие в процессах обмена.
Причины гиперинсулинизма могут длительное время никак себя не проявлять, но при этом губительно сказываются на работе всего организма.
Группы риска
Развитию гиперинсулинемии чаще всего подвержены следующие группы людей:
- женщины, у которых выявлен поликистоз яичников;
- люди, имеющие генетическую наследственность к этому заболеванию;
- пациенты с нарушениями в работе нервной системы;
- женщины, находящиеся в преддверии менопаузы;
- пожилые люди;
- пациенты, ведущие малоактивный образ жизни;
- женщины и мужчины, получающие гормональную терапию или препараты из группы бета-блокаторов.
Симптомы гиперинсулинизма
Заболевание способствует резкому набору массы тела, поэтому большинство диет оказываются неэффективными. Жировые отложения у женщин образуются в зоне талии, а также брюшной полости. Это вызвано большим депо инсулина, хранящегося в форме специфического жира (триглицерида).
Проявления гиперинсулинизма во многом схожи с признаками, развивающимися на фоне гипогликемии. Начало приступа характеризуется повышением аппетита, слабостью, потливостью, тахикардией и ощущением голода.
Впоследствии присоединяется паническое состояние, при котором отмечается присутствие страха, тревоги, дрожи в конечностях и раздражительности. Затем возникают дезориентация на местности, онемение в конечностях, возможно появление судорог. Отсутствие лечения может привести к потере сознания и коме.
- Легкая. Она характеризуется отсутствием каких-либо признаков в периоды между приступами, но при этом продолжает органически поражать кору головного мозга. Пациент отмечает ухудшение состояния не менее 1 раза на протяжении календарного месяца. Для купирования приступа достаточно применить соответствующие лекарственные препараты или употребить сладкую пищу.
- Средняя. Частота возникновения приступов – несколько раз в месяц. Человек может потерять сознание в этот момент или впасть в кому.
- Тяжелая. Такая степень болезни сопровождается необратимыми поражениями головного мозга. Приступы часто возникают и практически всегда приводят к потере сознания.
Проявления гиперинсулизма практически не отличаются у детей и взрослых людей. Особенностью течения болезни у маленьких пациентов является развитие приступов на фоне более низких показателей гликемии, а также высокая частота их повторения. Результатом постоянных обострений и регулярного купирования такого состояния препаратами становится нарушение психического здоровья у детей.
Чем опасно заболевание?
Любая патология может привести к осложнениям, если своевременно не предпринимать никаких действий. Гиперинсулинемия не является исключением, поэтому также сопровождается опасными последствиями. Заболевание протекает в острой и хронической формах. Пассивное течение приводит к притуплению мозговой деятельности, негативно влияет на психосоматическое состояние.
- нарушения в функционировании систем и внутренних органов;
- развитие диабета;
- ожирение;
- кома;
- отклонения в работе сердечно-сосудистой системы;
- энцефалопатия;
- паркинсонизм
Гиперинсулинемия, возникшая в детском возрасте, отрицательно сказывается на развитии ребенка.
Диагностика
Выявить болезнь часто бывает сложно из-за отсутствия специфических симптомов.
При обнаружении ухудшения самочувствия требуется консультация врача, который сможет определить источник такого состояния с помощью следующих диагностических исследований:
- анализ на гормоны, вырабатываемые гипофизом и поджелудочной железой;
- МРТ гипофиза, чтобы исключить онкологию;
- УЗИ брюшной полости;
- измерение давления;
- проверка уровня гликемии.
Постановка диагноза осуществляется на основе анализа полученных результатов обследования и жалоб пациента.
Лечение болезни
Терапия зависит от особенностей течения болезни, поэтому отличается в периоды обострения и ремиссии. Для купирования приступов требуется применение препаратов, а в остальное время достаточно соблюдать диету и проводить лечение основной патологии (диабета).
Помощь при обострении:
- съесть углевод или выпить сладкую воду, чай;
- струйно ввести раствор глюкозы, чтобы стабилизировать состояние (максимальное количество – 100 мл/1 раз);
- при наступлении комы нужно выполнить внутривенное введение глюкозы;
- при отсутствии улучшений следует сделать инъекцию адреналина или же глюкагона;
- применить транквилизаторы при судорогах.
Больные, находящиеся в тяжелом состоянии, должны быть доставлены в стационар и проходить лечение под наблюдением врачей. При органическом поражении железы может потребоваться резекция органа и проведение хирургического вмешательства.
Диета при гиперинсулинемии подбирается с учетом тяжести течения заболевания. Частые и сложно поддающиеся купированию приступы предусматривают присутствие повышенного количества углеводов в ежедневном рационе (до 450 г). Потребление жиров и белковой пищи при этом должно сохраняться в пределах нормы.
При нормальном течении болезни максимальное количество углеводов, поступивших с пищей за сутки, не должно превышать 150 г. Сладости, кондитерские изделия, алкоголь должны быть исключены из рациона.
Видео от эксперта:
Для сокращения проявлений гиперинсулинемии важно постоянно держать под контролем течение диабета и следовать основным рекомендациям:
- дробно и сбалансировано питаться;
- постоянно проверять уровень гликемии, корректировать ее при необходимости;
- соблюдать нужный питьевой режим;
- вести здоровый и активный образ жизни.
Если же чрезмерное производство инсулина стало следствием конкретного заболевания, то основная профилактика развития приступов сводится к лечению патологии, выступающей в роли основной причины их появления.
Абсолютный рост уровня инсулина в крови, или гиперинсулинизм: симптомы, диагностика и лечение
Гиперинсулинизм является заболеванием, которое протекает в виде гипогликемии, что представляет собой превышение нормы либо абсолютный рост уровня инсулина в крови.
Избыток данного гормона вызывает очень сильное повышение содержания сахара, что влечёт собой дефицит глюкозы, а также вызывает кислородное голодание головного мозга, которое ведёт к нарушениям нервной деятельности.
Возникновение и симптомы
Данное заболевание встречается чаще у женщин и протекает в возрасте от 26 до 55 лет. Приступы гипогликемии, как правило, проявляют себя утром после достаточно длительного голодания. Недуг может быть функциональным и проявляется он в такое же время суток, однако, после приёма углеводов.
Спровоцировать гиперинсулинизм может не только длительное голодание. Еще важными факторами проявления болезни вполне могут быть различные физические нагрузки и психические переживания. У женщин повторные симптомы заболевания могут возникнуть только в предменструальный период.
Гиперинсулинизм симптомы имеет следующие:
- непрерывное чувство голода;
- повышенное потоотделение;
- общая слабость;
- тахикардия;
- бледность;
- парестезия;
- диплопия;
- необъяснимое чувство страха;
- психическое возбуждение;
- тремор рук и дрожание конечностей;
- немотивированные действия;
- дизартрия.
Однако данные симптомы являются начальными, а если не лечить их и продолжать игнорировать заболевание дальше, то последствия могут оказаться более тяжёлыми.
Абсолютный гиперинсулинизм проявляется следующими симптомами:
- внезапная потеря сознания;
- кома с гипотермией;
- кома с гипорефлексией;
- тонические судороги;
- клинические судороги.
Такие приступы обычно проявляются после внезапной потери сознания.
До наступления приступа, проявляются следующие признаки:
- снижение эффективности памяти;
- эмоциональная нестабильность;
- полное безразличие к окружающим;
- потеря привычных профессиональных навыков;
- парестезия;
- симптомы пирамидной недостаточности;
- патологические рефлексы.
Причины возникновения
Вызвавшие гиперинсулинизм причины у взрослых и детей разделяют на две формы заболевания:
- панкреатический. Данная форма заболевания развивает абсолютную гиперинсулинемию. Она встречается как при злокачественных, так и при доброкачественных новообразованиях, а также гиперплазии бета-клеток поджелудочной железы;
- непанкреатический. Данная форма заболевания вызывает повышенный уровень инсулина.
Непанкреатическая форма заболевания развивается при таких состояниях:
- эндокринные заболевания. Они приводят к снижению контринсулиновых гормонов;
- поражение печени различной этиологии. Заболевания печени приводят к понижению уровня гликогена, а также нарушают обменные процессы и сопутствует развитию гипогликемии;
- недостаток ферментов, которые принимают непосредственное участие в процессах, отвечающих за обмен глюкозы. Приводит к относительному гиперинсулинизму;
- бесконтрольный приём препаратов, направленных на снижение уровня сахара при сахарном диабете. Может вызвать медикаментозную гипогликемию;
- нарушения в режиме питания. К данному состоянию относится: продолжительный период голодания, повышенная потеря жидкости и глюкозы (из-за рвоты, лактации, поноса), усиленные физические нагрузки без употребления углеводной пищи, что вызывает быстрое снижение уровня сахара в крови, употребление в пищу достаточно большого количества рафинированных углеводов, что значительно повышает уровень сахара в крови.
Патогенез
Глюкоза представляет собой, пожалуй, самый главный питательный субстрат центральной нервной системы человека и обеспечивает нормальное функционирование головного мозга.
Гипогликемия способна вызвать торможение метаболических, а также энергетических процессов.
Из-за нарушения окислительно-восстановительного процесса в организме происходит уменьшение потребления кислорода клетками коры головного мозга, из-за чего развивается гипоксия.
Гипоксия мозга проявляющаяся как: повышенная сонливость, апатия и торможение. В дальнейшем из-за недостатка глюкозы происходит нарушение всех обменных процессов в организме человека, а также значительное увеличение притока крови к мозгу, возникает спазм периферических сосудов, из-за чего нередко случается инфаркт.
Классификация болезни
Осложнения
Ранние возникают через небольшой промежуток времени после приступа, к ним относят:
Происходит это из-за очень резкого снижения метаболизма сердечной мышцы и головного мозга человека. Тяжёлый случай может спровоцировать развитие гипогликемической комы.
Поздние осложнения начинают проявляться по истечении достаточно длительного промежутка времени. Обычно через несколько месяцев, либо по истечении двух-трёх лет. Характерными признаками поздних осложнения являются паркинсонизм, энцефалопатия, нарушение памяти и речи.
Гиперинсулинизм: лечение и профилактика
В зависимости от причин, которые привели к появлению гиперинсулинемии, определяется тактика лечения заболевания. Так, в случае органического генеза назначают хирургическую терапию.
Она заключается в энуклеации новообразования, частичной резекции поджелудочной железы или же тотальной панкреатэктомии.
Как правило, после операционного вмешательства у больного наблюдается транзиторная гипергликемия, поэтому проводится последующее медикаментозное лечение и низкоуглеводная диета. Нормализация наступает спустя месяц после операции.
В случаях неоперабельных опухолей назначается паллиативная терапия, которая направлена на профилактику гипогликемии. Если у больного присутствуют злокачественные новообразования, то ему дополнительно необходима химиотерапия.
Если у пациента наблюдается функциональный гиперинсулинизм, то первоначальным является лечение, направленное на то заболевание, которое его вызвало.
При тяжёлых приступах заболевания с последующим развитием комы терапия осуществляется в реанимационных отделениях, проводится дезинтоксикационная инфузионная терапия, вводится адреналин и глюкокортикоиды. В случаях судорог и при психомоторном перевозбуждении показаны седативные препараты и инъекции транквилизаторов.
Видео по теме
Что такое гиперинсулинизм и как избавиться от постоянного чувства голода, можно узнать и этого видео:
Можно сказать про гиперинсулинизм, что это заболевание, которое может привести к тяжёлым осложнениям. Оно протекает в виде гипогликемии. По сути, данная болезнь является полной противоположностью сахарного диабета, ведь при нём наблюдается слабая выработка инсулина либо полное её отсутствие, а при гиперинсулинизме - повышенная или абсолютная. В основном данный диагноз ставится женской части населения.
- Устраняет причины нарушения давления
- Нормализует давление в течение 10 минут после приема
Гиперинсулинемия – явление патологического характера, которое по сути является увеличением количества инсулина в составе крови. Причины могут быть связаны с различными нарушениями, происходящими в организме, но результат один – скачок пептидного гормона, который вырабатывает поджелудочная железа. Что известно о гиперинсулинемии и как можно избежать подобного явления?
Почему развивается заболевание?
Специалисты выделяют следующие причины, которые приводят к возникновению патологии:
- поджелудочная железа начинает вырабатывать чрезмерное количество инсулина;
- чувствительность инсулиновых рецепторов снижается – возникает инсулинорезистентность;
- процесс переноса глюкозных молекул нарушается;
- происходят сбои при передаче сигналов в клеточной системе (определенные рецепторы не работают, поэтому у глюкозы нет возможности проникать в клетки).
Кроме этого, есть ряд предрасполагающих к гиперинсулинемии факторов.
Риски повышаются у следующих пациентов:
- обладающих наследственной предрасположенностью и имеющих родственников, страдающих сахарным диабетом;
- при нарушении центра регулирования таких чувств, как голод и насыщение;
- чаще диагностируется у женщин, особенно страдающих гормональными нарушениями, если поставлен диагноз синдром поликистозных яичников, а также при гестационном диабете;
- у людей, которые не проявляют физическую активность;
- при наличии пагубных привычек;
- у людей пожилого возраста;
- на фоне ожирения – излишняя жировая ткань приводит к тому, что рецепторы утрачивают восприимчивость к действию инсулина, и его синтез снижается;
- у пациентов, страдающих атеросклерозом;
- во время климактерического периода;
- при артериальной гипертензии;
- на фоне лечения гормональными препаратами, тиазидными диуретиками, бета-блокаторами.
Воздействие вредных веществ также негативно отражается на работе эндокринной системы
Подобные явления негативно отражаются на передаче сигналов в клетки. Резкое повышение инсулина может привести к развитию сахарного диабета, ожирению, гипогликемической коме. Кроме того, возникают риски нарушений в работе сердечно-сосудистой системы.
Как проявляется заболевание?
Симптомы при начальном развитии болезни отсутствуют, но после возникают явные признаки патологического нарушения:
- появление жировых отложений в области живота и верхней части туловища;
- приступы гипертонии;
- ощущение жажды;
- боли в мышечных тканях;
- головокружение;
- нарушение концентрации внимания;
- дрожь и озноб.
 При гиперинсулинемии человек становится слабым, вялым, быстро устает
При гиперинсулинемии человек становится слабым, вялым, быстро устает
Если увеличение инсулина возникает из-за генетического синдрома или редкого заболевания, тогда проявляются и другие симптомы:
- нарушается зрение;
- кожные покровы темнеют, возникает сухость;
- на коже живота и бедер образуются заметные растяжки;
- больного беспокоит затрудненная дефекация;
- беспокоит болезненность в костях.
Гиперинсулинемия – серьезное состояние, которое требует обязательной врачебной консультации.
Особенности диагностирования заболевания
Высокий уровень инсулина в крови влияет на различные системы организма и связан с разными заболеваниями, поэтому рекомендована комплексная диагностика.
Таблица № 1. Диагностические мероприятия для выявления гиперинсулинемии
| Анализ или обследование | Область исследования и особенности |
| Анализ на выявление определенных гормонов | Специалистов интересует уровень:
|
| Измерение артериального давления | Назначается суточный мониторинг – к телу пациента крепят специальный регистратор, оснащенный датчиком, который фиксирует появление и исчезновение пульсовых волн. |
| Вычисление особенностей конституции | Специалист определяет индекс массы тела (соотношение веса и роста), Также во внимание берется отношение окружностей талии и бедер. |
| Общий анализ мочи | Определяет микроальбуминурию – наличие в моче небольшого количества белка, которого в норме здесь быть не должно. |
| Ультразвуковое исследование | Обследуется поджелудочная железа, печень, почки. |
| Биохимия крови | Специалистов интересует уровень общего холестерина, триглицеридов, липопротеидов низкой и высокой плотности. Также анализ выявляет количество глюкозы на «голодный» желудок и после приема пищи. |
| КТ (кардиотокография); МРТ (магнитно-резонансная томография) | Исследуются гипофиз и кора надпочечников. Диагностика назначается, чтобы исключить наличие синдрома гиперкортицизма (болезни Иценко-Кушинга). |
Как лечится заболевание?
В общем-то, как при сахарном диабете, на первом месте в терапии этого заболевания находится диета, направленная на избавление от лишних килограммов – не красоты ради, а больше для здоровья.
 В основе питания лежит уменьшение калорийности употребляемой пищи
В основе питания лежит уменьшение калорийности употребляемой пищи
При составлении рациона учитывается несколько факторов:
- каким видом работы занимается пациент (умственным или физически трудом);
- занимается или нет спортом;
- вес на время обращения к специалисту и др.
Прием пищи сделать дробным – кушать 4-6 раз в день маленькими порциями.
При недостаточных физических нагрузках их следует увеличить, это сделает лечение более эффективным. Однако здесь существуют некоторые нюансы – статистическая силовая нагрузка может негативно отразиться на состоянии больного и стать причиной гипертонического криза. Поэтому при гиперинсулинемии лучше выбирать другие занятия.
 Для людей, страдающих резкими повышениями глюкозы в крови, больше подходит йога, пилатес, плавание, аэробика, аквааэробика и т.п
Для людей, страдающих резкими повышениями глюкозы в крови, больше подходит йога, пилатес, плавание, аэробика, аквааэробика и т.п
Коррекция питания и правильно подобранные тренировки, которые основаны на постепенном возрастании нагрузки, являются залогом улучшения состояния пациента.
Кроме того, лечение также может включать прием медикаментозных средств.
Таблица № 2. Препараты, назначаемые при гиперинсулинемии, и их действие
| Тип лекарств | Действие |
| Гипогликемические препараты: бигуаниды, тиазолидины | Лекарственные средства, которые снижают уровень сахара в крови. |
| Препараты с антигипертензивным действием | Назначаются для нормализации артериального давления, также, благодаря их приему, удается избежать развития инфарктов, инсультов. |
| Ингибиторы АПФ | Используются для лечения артериальной гипертензии – снижают как систолическое, так и диастолическое давление. |
| Станины и фибраты | Средства, эффективно снижающие уровень холестерина. |
| Ингибиторы обратного захвата серотонина | Лекарственные средства, которые снижают аппетит. |
| Препараты, содержащие альфа-лиоевую кислоту | Повышают утилизацию излишков глюкозы и выводят из организма лишний холестерин. |
Профилактические меры
Гиперинсулинемия – одно из тех заболеваний, которые, в большинстве случаев, можно предотвратить, если придерживаться простых правил:
- не употреблять чрезмерно жирную и сладкую пищу;
- включить в рацион побольше овощей и фруктов зеленого цвета;
- обеспечивать себя достаточными нагрузками – минимум ходить ежедневно в течение получаса;
- отказаться от пагубных привычек, негативно отражающихся на состоянии здоровья.
Данное заболевание является высоким фактором риска развития более серьезных болезней и состояний – сахарных диабетов, инсультов, инфарктов. Поэтому желательно выявлять недуг как можно раньше и своевременно лечить его.