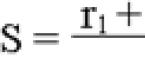Вконтакте
Одноклассники
– потенциально обратимое, внезапно наступившее выраженное нарушение или прекращение функции почек. Характерно нарушение всех почечных функций (секреторной, выделительной и фильтрационной), выраженные изменения водно-электролитного баланса, быстро нарастающая азотемия. В развитии ОПН выделяют 4 последовательные фазы: начальную, олигоанурическую, диуретическую и период выздоровления. Диагностика осуществляется по данным клинических и биохимических анализов крови и мочи, а также инструментальных исследований мочевыделительной системы. Лечение зависит от стадии острой почечной недостаточности. Оно включает симптоматическую терапию, методы экстракорпоральной гемокоррекции, поддержание оптимального артериального давления и диуреза.
Острая почечная недостаточность – потенциально обратимое, внезапно наступившее выраженное нарушение или прекращение функции почек. Характерно нарушение всех почечных функций (секреторной, выделительной и фильтрационной), выраженные изменения водно-электролитного баланса, быстро нарастающая азотемия.
Выделяют следующие формы ОПН:
- Гемодинамическая (преренальная). Возникает вследствие острого нарушения гемодинамики.
- Паренхиматозная (ренальная). Причиной становится токсическое или ишемическое поражение почечной паренхимы, реже – острый воспалительный процесс в почках.
- Обструктивная (постренальная). Развивается вследствие остро возникшей обструкции мочевыводящих путей.
Этиология преренальной ОПН
Преренальная ОПН может развиваться при состояниях, которые сопровождаются снижением сердечного выброса (при тромбоэмболии легочной артерии, сердечной недостаточности, аритмии, тампонаде сердца, кардиогенном шоке). Нередко причиной становится уменьшение количества внеклеточной жидкости (при диарее, дегидратации, острой кровопотере, ожогах, асците, вызванном циррозом печени). Может возникать вследствие выраженной вазодилатации, возникающей при бактериотоксическом или анафилактическом шоке.
Этиология ренальной ОПН
Возникает при токсическом воздействии на почечную паренхиму удобрений, ядовитых грибов, солей меди, кадмия, урана и ртути. Развивается при бесконтрольном приеме нефротоксичных медикаментов (противоопухолевые препараты, ряд антибиотиков и сульфаниламидов). Рентгенконстрастные вещества и перечисленные препараты, назначенные в обычной дозировке, могут стать причиной ренальной ОПН у больных с нарушением функции почек.
Кроме того, данная форма ОПН возникает при циркуляции в крови большого количества миоглобина и гемоглобина (при выраженной макрогемаглобинурии, переливании несовместимой крови, длительном сдавлении тканей при травме, наркотической и алкогольной коме). Реже развитие ренальной ОПН обусловлено воспалительным заболеванием почек.
Этиология постренальной ОПН
Развивается при механическом нарушении пассажа мочи при двухсторонней обструкции мочевых путей камнями. Реже возникает при опухолях предстательной железы, мочевого пузыря и мочеточников, туберкулезном поражении, уретритах и периуретритах, дистрофических поражениях забрюшинной клетчатки.
При тяжелых сочетанных травмах и обширных хирургических вмешательствах острая почечная недостаточность вызывается несколькими факторами (шок, сепсис, переливание крови, лечение нефротоксичными препаратами).
Симптомы ОПН
Выделяют четыре фазы острой почечной недостаточности:
Состояние пациента определяется основным заболеванием, вызывающим ОПН. Клинически начальная фаза обычно не выявляется из-за отсутствия характерных симптомов. Циркуляторный коллапс, возникающий в этой фазе, имеет очень малую продолжительность, поэтому проходит незамеченным. Неспецифичные симптомы ОПН (сонливость, тошнота, отсутствие аппетита, слабость) замаскированы проявлениями основного заболевания, травмы или отравления.
Анурия возникает редко. Количество отделяемой мочи — менее 500 мл в сутки. Характерна выраженная протеинурия, азотемия, гиперфосфатемия, гиперкалиемия, гипернатиемия, метаболический ацидоз. Отмечается понос, тошнота, рвота. При отеке легкого вследствие гипергидратации появляется одышка и влажные хрипы. Больной заторможен, сонлив, может впасть в кому. Нередко развивается перикардит, уремический гастроэнтероколит, осложняющийся кровотечениями. Пациент подвержен инфекции вследствие снижения иммунитета. Возможен панкреатит, стоматит паротит, пневмония, сепсис.
Олигоанурическая фаза ОПН развивается в течение первых трех суток после воздействия. Позднее развитие олигоанурической фазы считается прогностически неблагоприятным признаком. Средняя продолжительность этой стадии 10-14 дней. Период олигурии может укорачиваться до нескольких часов или удлиняться до 6-8 недель. Продолжительная олигурия чаще возникает у пожилых пациентов с сопутствующей сосудистой патологией. При олигурической стадии ОПН, длящейся более месяца, необходимо провести дополнительную дифференциальную диагностику для исключения прогрессирующего гломерулонефрита, почечного васкулита, окклюзии почечной артерии, диффузного некроза коры почек.
Длительность диуретической фазы – около двух недель. Суточный диурез постепенно увеличивается и достигает 2-5 литров. Отмечается постепенное восстановление водно-электролитного баланса. Возможна гипокалиемия вследствие значительных потерь калия с мочой.
Происходит дальнейшее восстановление почечных функций, занимающее от 6 месяцев до 1 года.
Осложнения ОПН
Выраженность нарушений, характерных для почечной недостаточности (задержка жидкости, азотемия, нарушение водно-электролитного баланса) зависит от состояния катаболизма и наличия олигурии. При выраженной олигурии отмечается снижение уровня клубочковой фильтрации, существенно уменьшается выделение электролитов, воды и продуктов азотного обмена, что приводит к более выраженным изменениям состава крови.
При олигурии увеличивается риск развития водной и солевой сверхнагрузки. Гиперкалиемия при острой почечной недостаточности вызвана недостаточным выведением калия при сохраняющемся уровне его высвобождения из тканей. У больных, не страдающих олигурией, уровень калия составляет 0,3-0,5 ммоль/сут. Более выраженная гиперкалиемия у таких пациентов может говорить об экзогенной (переливание крови, лекарственные препараты, наличие в рационе продуктов, богатых калием) или энодгенной (гемолиз, деструкция тканей) калиевой нагрузке.
Первые симптомы гиперкалиемии появляются, когда уровень калия превышает 6,0-6,5 ммоль/л. Больные жалуются на мышечную слабость. В некоторых случаях развивается вялый тетрапарез. Отмечаются изменения ЭКГ. Снижается амплитуда зубцов P, увеличивается интервал P-R, развивается брадикардия. Значительное повышение концентрации калия может вызвать остановку сердца.
На первых двух стадиях ОПН наблюдаются гипокальциемия, гиперфосфатемия, слабо выраженная гипермагниемия.
Следствием выраженной азотемии является угнетение эритропоэза. Сокращается продолжительность жизни эритроцитов. Развивается нормоцитарная нормохромная анемия.
Угнетение иммунитета способствует возникновению инфекционных заболеваний у 30-70% пациентов с острой почечной недостаточностью. Присоединение инфекции утяжеляет течение заболевания и нередко становится причиной смерти больного. Развивается воспаление в области послеоперационных ран, страдает полость рта, дыхательная система, мочевыводящие пути. Частым осложнением острой почечной недостаточности является сепсис, который может вызываться как грамположительной, так и грамотрицательной флорой.
Отмечается сонливость, спутанность сознания, дезориентация, заторможенность, чередующаяся с периодами возбуждения. Периферическая нейропатия чаще возникает у пожилых пациентов.
- Осложнения со стороны сердечно-сосудистой системы
При ОПН может развиться застойная сердечная недостаточность, аритмия, перикардит, артериальная гипертензия.
Больных беспокоит ощущение дискомфорта в брюшной полости, тошнота, рвота, потеря аппетита. В тяжелых случаях развивается уремический гастроэнтероколит, часто осложняющийся кровотечениями.
Диагностика ОПН
Основным маркером острой почечной недостаточности является повышение калия и азотистых соединений в крови на фоне значительного уменьшения количества выделяемой организмом мочи вплоть до состояния анурии. Количество суточной мочи и концентрационную способность почек оценивают по результатам пробы Зимницкого. Важное значение имеет мониторинг таких показателей биохимии крови, как мочевина, креатинин и электролиты. Именно эти показатели позволяют судить о тяжести острой почечной недостаточности и эффективности проводимых лечебных мероприятий.
Главной задачей в диагностике ОПН является определение ее формы. Для этого проводится УЗИ почек и мочевого пузыря, которое позволяет выявить или же исключить обструкцию мочевыводящих путей. В некоторых случаях проводится двусторонняя катетеризация лоханок. Если при этом оба катетера свободно прошли в лоханки, но выделение мочи по ним не наблюдается, можно с уверенностью исключить постренальную форму острой почечной недостаточности.
При необходимости оценить почечный кровоток проводят УЗДГ сосудов почек. Подозрение на канальцевый некроз, острый гломерулонефрит или системное заболевание является показанием для биопсии почки.
Лечение ОПН
Лечение в начальной фазе
Терапия направлена, прежде всего, на устранение причины, которая вызвала нарушение функции почек. При шоке необходимо восполнить объем циркулирующей крови и нормализовать артериальное давление. При отравлении нефротоксинами больным промывают желудок и кишечник. Применение в урологии таких современных методов лечения как экстракорпоральная гемокоррекция позволяет быстро очистить организм от токсинов, которые стали причиной развития острой почечной недостаточности. С этой целью проводят гемосорбцию и плазмаферез. При наличии обструкции восстанавливают нормальный пассаж мочи. Для этого проводят удаление камней из почек и мочеточников, оперативное устранение стриктур мочеточников и удаление опухолей.
Лечение в фазе олигурии
Для стимуляции диуреза больному назначают фуросемид и осмотические диуретики. Для уменьшения вазоконстрикции почечных сосудов вводят допамин. Определяя объем вводимой жидкости, кроме потерь при мочеиспускании, рвоте и опорожнении кишечника, необходимо учитывать потери при потоотделении и дыхании. Пациента переводят на безбелковую диету, ограничивают поступление калия с пищей. Проводится дренирование ран, удаление участков некроза. При выборе дозы антибиотиков следует учитывать тяжесть поражения почек.
Показания к гемодиализу
Гемодиализ проводится при повышении уровня мочевины до 24 ммоль/л, калия – до 7 ммоль/л. Показанием к гемодиализу являются симптомы уремии, ацидоз и гипергидратация. В настоящее время для предупреждения осложнений, возникающих вследствие нарушений метаболизма, нефрологи все чаще проводят ранний и профилактический гемодиализ.
Летальность в первую очередь зависит от тяжести патологического состояния, ставшего причиной развития ОПН. На исход заболевания влияет возраст больного, степень нарушения функции почек, наличие осложнений. У выживших пациентов почечные функции восстанавливаются полностью в 35-40% случаев, частично – в 10-15% случаев. 1-3% больных необходим постоянный гемодиализ.
Острая почечная недостаточность (ОПН) развивается как осложнение многих заболеваний и патологических процессов. Острая почечная недостаточность – синдром, развивающийся в результате нарушения почечных процессов (почечного кровотока, клубочковой фильтрации, канальцевой секреции, канальцевой реабсорбции, концентрационной способности почек) и характеризующийся азотемией, нарушениями водно-электролитного равновесия и кислотно-основного состояния.
Острая почечная недостаточность может быть обусловлена преренальными, ренальными и постренальными нарушениями. Преренальная ОПН развивается в связи с нарушением почечного кровотока, ренальная ОПН – при поражении почечной паренхимы, постренальная ОПН связана с нарушением оттока мочи.
Морфологическим субстратом ОПН является острый тубулонекроз, проявляющийся уменьшением высоты щеточной каймы, снижением складчатости базолатеральных мембран, некрозом эпителия.
Преренальная острая почечная недостаточность характеризуется снижением почечного кровотока в результате вазоконстрикции афферентных артериол в условиях нарушения системной гемодинамики и уменьшения объема циркулирующей крови, функция почки при этом сохранена.
длительное или кратковременное (реже) снижение артериального давления ниже 80 мм рт.ст. (шок, обусловленный разными причинами: постгеморрагический, травматический, кардиогенный, септический, анафилактический и др., обширные оперативные вмешательства);
уменьшение объема циркулирующей крови (кровопотеря, плазмопотеря, неукротимые рвоты, поносы);
увеличение внутрисосудистой емкости, сопровождающееся снижением периферического сопротивления (септицемия, эндотоксинемия, анафилаксия);
уменьшение сердечного выброса (инфаркт миокарда, сердечная недостаточность, эмболия легочной артерии).
Ключевым звеном патогенеза преренальной ОПН является резкое снижение уровня клубочковой фильтрации вследствие спазма афферентных артериол, шунтирования крови в юкстагломерулярном слое и ишемии коркового слоя под влиянием повреждающего фактора. В связи с уменьшением объема перфузируемой через почки крови клиренс метаболитов снижается и развивается азотемия . Поэтому некоторые авторы называет этот вид ОПН преренальной азотемией. При длительном снижении почечного кровотока (более 3 дней) преренальная ОПН переходит в ренальную ОПН.
Степень ишемии почек коррелирует со структурными изменениями эпителия проксимальных канальцев (уменьшение высоты щеточной каймы и площади базолатеральных мембран). Начальная ишемия способствует увеличению проницаемости мембран клеток канальцевого эпителия для ионов, который поступает в цитоплазму, активно транспортируется специальным переносчиком на внутреннюю поверхность мембран митохондрий или в саркоплазматический ретикулум. Развивающийся в клетках дефицит энергии вследствие ишемии и потребления энергии при перемещении ионов приводит к некрозу клеток, а образовавшийся клеточный детрит обтурирует канальцы, усугубляя тем самым анурию. Объем канальцевой жидкости в условиях ишемии уменьшен.
Повреждение нефроцитов сопровождается нарушением реабсорбции натрия в проксимальных канальцах и избыточным поступлением натрия в дистальные отделы. Натрий стимулирует в macula densa продукцию ренина, у больных с ОПН его содержание, как правило, повышено. Ренин активирует ренин-ангиотензин-альдостероновую систему. Тонус симпатических нервов и продукция катехоламинов повышены. Под влиянием компонентов системы ренин-апгиотензин-альдостерон и катехоламинов поддерживается афферентная вазоконстрикция и ишемия почки. В капиллярах клубочков давление падает и, соответственно, снижается эффективное фильтрационное давление.
При резком ограничении перфузии коркового слоя кровь попадает в капилляры юкстагломерулярной зоны («Оксфордский шунт»), в которых возникает стаз. Повышение давления в канальцах сопровождается снижением клубочковой фильтрации. Гипоксия наиболее чувствительных к ней дистальных канальцев проявляется некрозом канальцевого эпителия и базальной мембраны вплоть до тубулярного некроза. Происходит обтурация канальцев фрагментами некротизированных эпителиальных клеток, цилиндрами и др.
В условиях гипоксии в мозговом слое изменение активности ферментов арахидонового каскада сопровождается уменьшением образования простагландинов, обладающих вазодилататорным действием, и выделением биологически активных веществ (гистамин, серотонин, брадикинин), непосредственно влияющих на сосуды почек и нарушающих почечную гемодинамику. Это, в свою очередь, способствует вторичному повреждению почечных канальцев.
После восстановления почечного кровотока происходит образование активных форм кислорода, свободных радикалов и активация фосфолипазы, что поддерживает нарушения проницаемости мембран для ионов и пролонгирует олигурическую фазу ОПН. В последние годы для устранения нежелательного кальциевого транспорта в клетки на ранних этапах ОПН, даже на фоне ишемии или непосредственно после ее устранения, применяют блокаторы кальциевых каналов (нифедипин, верапамил). Синергический эффект наблюдается при применении ингибиторов кальциевых каналов в сочетании с веществами, способными улавливать свободные радикалы, например глутатион. Ионы, адениннуклеотиды предохраняют митохондрии от повреждения.
Степень ишемии почки коррелирует со структурными изменениями эпителия канальцев, возможно развитие вакуольной дистрофии или некроза отдельных нефроцитов. Вакуольная дистрофия устраняется в течение 15 дней после прекращения действия повреждающего фактора.
Ренальная острая почечная недостаточность развивается вследствие ишемии почки, то есть возникает вторично при первично нарушенной перфузии почки или под действием следующих причин:
воспалительный процесс в почках (гломерулонефрит, интерстициальный нефрит, васкулит);
эндо- и экзотоксины (лекарственные препараты, рентгеноконтрастные вещества, соли тяжелых металлов – соединения ртути, свинца, мышьяка, кадмия и др., органические растворители, этиленгликоль, четыреххлористый углерод, яды животного и растительного происхождения;
реноваскулярные заболевания (тромбоз и эмболия почечной артерии, расслаивающая аневризма аорты, двухсторонний тромбоз почечных вен);
пигментемия – гемоглобинемия (внутрисосудистый гемолиз) и миоглобинемия (травматический и нетравматический рабдомиолиз);
Для этого типа ОПН характерен острый канальцевый некроз, вызванный ишемией или нефротоксинами, которые фиксируются на клетках почечных канальцев. В первую очередь повреждаются проксимальные канальцы, происходит дистрофия и некроз эпителия, в последующем – умеренные изменения интерстиция почек. Клубочковые повреждения, как правило, незначительны.
К настоящему времени описано более 100 нефротоксинов, оказывающих непосредственное повреждающее действие на клетки почечных канальцев (острый канальцевый некроз, нефроз нижнего отдела нефрона, вазомоторная вазопатия). Острой почечной недостаточностью, вызванной нефротоксинами, обусловлено около 10 % всех поступлений больных в центры острого гемодиализа.
Нефротоксины вызывают повреждение тубулоэпителиальных структур разной степени выраженности – от дистрофий (гидропическая, вакуольная, баллонная, жировая, гиалинокапельная) до парциального или массивного коагуляционного некроза нефроцитов. Эти изменения происходят в результате реабсорбции и депонирования в цитоплазме макро- и микрочастиц, а также фиксации на клеточной мембране и в цитоплазме нефротоксинов, фильтрующихся через гломерулярный фильтр. Возникновение той или иной дистрофии определяется действующим фактором.
Нефротоксичность ядов «тиоловой группы» (соединения ртути, хрома, меди, золота, кобальта, цинка, свинца, висмута, лития, урана, кадмия и мышьяка) проявляется блокадой сульфгидрильных (тиоловых) групп ферментативных и структурных белков и плазмокоагулирующим эффектом, что вызывает массивный коагуляционный некроз канальцев. Сулема вызывает избирательное поражение почек – «сулемовый нефроз». Другие вещества этой группы не отличаются избирательностью действия и повреждают ткань почек, печени и эритроциты. Например, особенностью отравлений медным купоросом, бихроматами, мышьяковистым водородом является сочетание коагуляционного некроза эпителия проксимальных канальцев с острым гемоглобинурийным нефрозом. При отравлениях бихроматами и мышьяковистым водородом наблюдается центролобулярный некроз печени с холемией и хелатурией.
Отравление этиленгликолем и его производными характеризуется необратимой деструкцией внутриклеточных структур, называемой баллонной дистрофией. Этиленгликоль и продукты его распада реабсорбируются клетками эпителия почечных канальцев, в них образуется большая вакуоль, которая смещает клеточные органеллы вместе с ядром к базальным отделам. Подобная дистрофия, как правило, завершается колликвационным некрозом и полным выпадением функции пораженных канальцев. Возможна также секвестрация поврежденной части клетки вместе с вакуолью, а сохранившиеся базальные отделы с оттесненным ядром могут быть источником регенерации.
Отравление дихлорэтаном, реже хлороформом, сопровождается жировой дистрофией нефроцитов (острый липидный нефроз) проксимальных, дистальных канальцев и петли Генле. Эти яды обладают прямым токсическим действием на цитоплазму, изменяя соотношения в ней белково-липидных комплексов, что сопровождается угнетением реабсорбции в канальцах.
Реабсорбция белковых пигментных агрегатов (гемоглобин, миоглобин) эпителиальными клетками проксимальных и дистальных канальцев вызывает гиалино-капельпую дистрофию. Пигментные белки, профильтровавшиеся через гломерулярный фильтр, продвигаются по канальцу и постепенно осаждаются на щеточной кайме в проксимальных канальцах, частично реабсорбируются нефроцитами. Накопление гранул пигмента в эпителиальных клетках сопровождается частичным разрушением апикальных отделов цитоплазмы и их секвестрацией в просвет канальцев вместе со щеточной каймой, где и формируются зернистые и глыбчатые пигментные цилиндры. Процесс разворачивается на протяжении 3-7 дней. В этот период нереабсорбированные пигментные массы в просвете канальцев уплотняются, перемещаются в петлю Генле и дистальные канальцы. В апикальных отделах эпителиальных клеток, перегруженных гранулами пигмента, происходит парциальный некроз. Отдельные гранулы пигмента преобразуются в ферритин и длительно задерживаются в цитоплазме.
Нефротоксичность аминогликозидов (канамицин, гентамицин, мономицин, неомицин, тобармицин и др.) связана с наличием в их молекулах свободных аминогрупп в боковых цепях. Аминогликозиды в организме не метаболизируются, и 99 % их в неизмененном виде выводится с мочой. Профильтровавшиеся аминогликозиды фиксируются на апикальной мембране клеток проксимальных канальцев и петли Генле, связываются с везикулами, поглощаются путем пиноцитоза и секвестрируются в лизосомах канальцевого эпителия. При этом концентрация препарата в корковом веществе становится выше, чем в плазме. Для поражения почек аминогликозидами характерно увеличение в мембранах анионных фосфолипидов, в частности, фосфатидилинозитола, повреждение мембран митохондрий, сопровождающееся потерей внутриклеточного калия и магния, нарушение окислительного фосфорилирования и дефицит энергии. Сочетание этих изменений приводит к некрозу канальцевого эпителия.
Характерно, что ионы препятствуют фиксации аминогликозидов на щеточной кайме и таким образом уменьшают их нефротоксичность. Отмечено, что канальцевый эпителий, регенерирующий после повреждения аминогликозидами, становится резистентным к токсическому влиянию этих препаратов.
Терапия осмотическими диуретинами (растворы глюкозы, мочевины, декстранов, маннитола и др.) может осложняться гидропической и вакуольной дистрофией нефроцитов. При этом в проксимальных канальцах изменяется осмотический градиент жидкостей по обе стороны канальцевой клетки – крови, омывающей канальцы, и провизорной мочи. Поэтому возможно перемещение воды в клетки канальцевого эпителия из перитубулярных капилляров или из провизорной мочи. Гидропия эпителиальных клеток при использовании осмотических диуретинов сохраняется длительное время и, как правило, связана с частичной реабсорбцией осмотически активных веществ и задержкой их в цитоплазме. Задержка воды в клетке резко снижает ее энергетический потенциал и функциональные возможности. Таким образом, осмотический нефроз является не причиной ОПН, а нежелательным эффектом ее лечения или следствием восполнения энергетических субстратов в организме парентеральным введением гипертонических растворов.
Состав мочи при ренальной ОПН близок по составу клубочковому фильтрату: низкий удельный вес, низкая осмолярность. Содержание в моче повышено из-за нарушения его реабсорбции.
Постренальная острая почечная недостаточность возникает вследствие нарушения оттока мочи по мочевыводящим путям в результате следующих нарушений:
окклюзии мочевыводящих путей конкрементами или сгустками крови;
обструкции мочеточников или мочеточника опухолью, располагающейся вне мочевыводящих путей;
Нарушение оттока мочи сопровождается перерастяжением мочевыводящих путей (мочеточники, лоханки, чашечки, собирательные трубки, канальцы) и включением системы рефлюксов. Происходит обратное затекание мочи из мочевыводящих путей в интерстициальное пространство почечной паренхимы (пиелоренальный рефлюкс). Но выраженного отека не наблюдается благодаря оттоку жидкости по системе венозных и лимфатических сосудов (пиеловенозный рефлюкс). Поэтому интенсивность гидростатического давления на канальцы и клубочек весьма умеренная, и фильтрация снижена незначительно. Выраженных нарушений околоканальцевого кровотока не происходит и, несмотря на анурию, функция почек сохранена. После устранения препятствия оттоку мочи диурез восстанавливается. Если продолжительность окклюзии не превышает трех суток, явления ОПН после восстановления проходимости мочевыводящих путей достаточно быстро исчезают.
При длительной окклюзии и высоком гидростатическом давлении нарушаются фильтрация и околоканальцевый кровоток. Эти изменения в сочетании с постоянными рефлюксами способствуют развитию интерстициального отека и канальцевого некроза.
Клиническое течение ОПН имеет определенную закономерность и стадийность независимо от причины, ее вызвавшей.
1-я стадия – короткая по продолжительности и заканчивается после прекращения действия фактора;
2-я стадия – период олигоанурии (объем выделяемой мочи не превышает 500 мл/сут.), азотемии; в случае длительной олигурии (до 4 нед.) резко повышается вероятность развития кортикального некроза;
3-я стадия – период полиурии – восстановление диуреза с фазой полиурии (объем выделяемой мочи превышает 1800 мл/сут.);
4-я стадия – восстановление функции почек. Клинически наиболее тяжело протекает 2-я стадия.
Развивается внеклеточная и внутриклеточная гипергидратация, негазовый выделительный почечный ацидоз (в зависимости от локализации повреждения канальцев возможен ацидоз 1-го, 2-го, 3-го типов). Первым признаком гипергидратации является одышка, обусловленная интерстициальным или кардиогенным отеком легких. Несколько позже жидкость начинает скапливаться в полостях, возникают гидроторакс, асцит, отеки нижних конечностей и в области поясницы. Это сопровождается резко выраженными изменениями биохимических показателей крови: азотемия (содержание креатинина, мочевины, мочевой кислоты повышено), гиперкалиемия, гипонатриемия, гипохлоремия, гипермагниемия, гиперфосфатемия.
Уровень креатинина крови повышается независимо от характера питания больного и интенсивности распада белка. Поэтому степень креатинемии дает представление о тяжести течения и прогнозе при ОПН. Степень катаболизма и некроза мышечной ткани отражает гиперурикемия.
Гиперкалиемия возникает в результате снижения экскреции калия, усиленного выхода калия из клеток, развивающегося почечного ацидоза. Гиперкалиемия 7,6 ммоль/л клинически проявляется нарушениями сердечного ритма вплоть до полной остановки сердца; возникает гипорефлексия, снижается возбудимость мышц с развитием в последующем мышечных параличей.
Электрокардиографические показатели при гиперкалиемии: зубец Т – высокий, узкий, линия ST сливается с зубцом Т; исчезновение зубца Р; уширение комплекса QRS.
Гиперфосфатемия вызвана нарушением выведения фосфатов. Генез гипокальциемии остается неясным. Как правило, сдвиги фосфорно-кальциевого гомеостаза протекают бессимптомно. Но при быстрой коррекции ацидоза у больных с гипокальциемией возможно возникновение тетании, судорог. Гипонатриемия связана с задержкой воды или избыточным ее введением. Абсолютного дефицита натрия в организме нет. Гиперсульфатемия, гипермагниемия, как правило, протекают бессимптомно.
В течение нескольких дней развивается анемия, генез которой объясняется гипергидратацией, гемолизом эритроцитов, кровотечениями, угнетением продукции эритропоэтина циркулирующими в крови токсинами. Обычно анемия сочетается с тромбоцитопенией.
Для второй стадии характерно появление признаков уремии, при этом преобладают симптомы со стороны желудочно-кишечного тракта (отсутствие аппетита, тошнота, рвота, метеоризм, диарея).
При назначении антибиотиков в начале симптомы диареи нарастают. В последующем диарея сменяется запорами вследствие резкой гипокинезии кишечника. В 10 % случаев наблюдаются желудочно-кишечные кровотечения (эрозии, язвы желудочно-кишечного тракта, нарушение свертываемости крови).
Своевременно назначенная терапия предупреждает развитие комы, уремического перикардита.
В период олигурической стадии (9-11 дней) моча темного цвета, выражена протеинурия и цилиндрурия, натрийурия не превышает 50 ммоль/л, осмолярность мочи соответствует осмолярности плазмы. У 10 % больных при остром лекарственном интерстициальном нефрите диурез сохранен.
3-я стадия характеризуется восстановлением диуреза к 12-15-м суткам от начала заболевания и полиурией (более 2 л/сутки), сохраняющейся в течение 3-4 недель. Генез полиурии объясняется восстановлением фильтрационной функции почек и недостаточной концентрационной функцией канальцев. В полиурическую стадию происходит разгрузка организма от жидкости, накопившейся в период олигурии. Вторично возможна дегидратация, гипокалиемия и гипонатриемия. Выраженность протеинурии снижается.
Дифференциальная диагностика преренальной и ренальной ОПН
Острая почечная недостаточность (ОПН) представляет собой внезапное нарушение функций обеих почек, вызванное снижением почечного кровотока и замедлением процессов клубочковой фильтрации и канальцевой реабсорбции. В результате происходит задержка или полное прекращение выведения из организма токсических веществ и расстройство кислотно-основного, электролитного и водного баланса.
При правильном и своевременном лечении эти патологические изменения являются обратимыми. По данным медицинской статистики ежегодно случаи ОПН регистрируются примерно у 200 человек на 1 миллион.
Формы и причины ОПН
В зависимости от того, какие процессы привели к возникновению острой почечной недостаточности, выделяют преренальную, ренальную и постренальную формы.
Преренальная форма ОПН
Преренальная форма ОПН характеризуется значительным сокращением почечного кровотока и снижением скорости клубочковой фильтрации. Такие нарушения в работе почек связаны с общим уменьшением объема циркулирующей крови в организме. В случае если нормальное кровоснабжение органа не будет восстановлено в кратчайшие сроки, возможны ишемия или некроз почечной ткани. Основными причинами развития преренальной ОПН являются:
- снижение сердечного выброса;
- тромбоэмболия легочной артерии;
- операции и травмы, сопровождающиеся значительной кровопотерей;
- обширные ожоги;
- обезвоживание, вызванное диареей, рвотой;
- прием мочегонных препаратов;
- внезапное снижение сосудистого тонуса.
Ренальная форма ОПН
При ренальной форме ОПН наблюдается поражение паренхимы почек. Оно может быть вызвано воспалительными процессами, токсическим действием или патологиями сосудов почек, которые приводят к недостаточности кровоснабжения органа. Ренальная ОПН является следствием некроза эпителиальных клеток канальцев почек. В результате происходит нарушение целостности канальцев и выход их содержимого в окружающие ткани почки. К развитию ренальной формы ОПН могут приводить следующие факторы:
- интоксикация различными ядами, лекарствами, рентгеноконтрастными соединениями, тяжелыми металлами, укусами змей или насекомых и др.;
- заболевания почек: интерстициальный нефрит, острый пиелонефрит и гломерулонефрит;
- поражение почечных сосудов (тромбоз, аневризма, атеросклероз, васкулит и др.);
- травмы почек.
Важно: Длительный прием лекарственных средств, оказывающих нефротоксическое действие, без предварительной консультации с врачом может стать причиной ОПН.
Постренальная ОПН
Постренальная ОПН развивается в результате острого нарушения пассажа мочи. При этой форме ОПН функция почек сохраняется, но процесс выделения мочи затруднен. Возможно возникновение ишемии почечной ткани, так как переполненные мочой лоханки начинают сдавливать окружающие ткани почки. К причинам возникновения постренальной ОПН относятся:
- спазм сфинктера мочевого пузыря;
- закупорка мочеточников вследствие мочекаменной болезни;
- опухоли мочевого пузыря, предстательной железы, мочевыводящих каналов, органов таза;
- травмы и гематомы;
- воспалительные заболевания мочеточников или мочевого пузыря.
Стадии и симптомы ОПН
Характерные симптомы ОПН развиваются очень быстро. Отмечается резкое ухудшение общего состояния пациента и нарушение почечной функции. В клинической картине острой почечной недостаточности выделяют стадии, для каждой из которых характерны определенные признаки:
- начальная стадия;
- стадия олигоанурии;
- стадия полиурии;
- стадия выздоровления.
На первой стадии ОПН симптомы определяются причиной заболевания. Это могут быть признаки интоксикации, шока или проявления какого-то заболевания. Так, при инфекционном поражении почек отмечается лихорадка, головная боль, мышечная слабость. В случае кишечной инфекции присутствует рвота и диарея. Для токсического поражения почек характерны проявления желтухи, анемия, возможны судороги. Если причиной ОПН является острый гломерулонефрит, то отмечается выделение мочи с примесью крови и боли в области поясницы. Для первой стадии ОПН характерно снижение артериального давления, бледность, учащенный пульс, незначительное уменьшение диуреза (до 10%).
Стадия олигоанурии при ОПН является самой тяжелой и представляет наибольшую опасность для жизни пациента. Она характеризуется следующими симптомами:
- резкое снижение или прекращение выделения мочи;
- интоксикация продуктами азотистого обмена, проявляющаяся в виде тошноты, рвоты, зуда кожных покровов, учащения дыхания, потери аппетита, тахикардии;
- повышение артериального давления;
- спутанность и потеря сознания, коматозное состояние;
- отеки подкожной клетчатки, внутренних органов и полостей;
- повышение массы тела за счет наличия избытка жидкости в организме;
- общее тяжелое состояние.
Дальнейшее течение ОПН определяется успешностью проведенной терапии на второй стадии. При благоприятном исходе наступает стадия полиурии и последующего выздоровления. Сначала наблюдается постепенное увеличение диуреза, а затем развивается полиурия. Из организма выводится избыточная жидкость, уменьшаются отеки, кровь очищается от токсических продуктов. Стадия полиурии может быть опасна возникновением обезвоживания и нарушениями электролитного баланса (например, гипокалиемией). Примерно через месяц диурез приходит в норму и начинается период выздоровления, который может длиться до 1 года.
Если лечение было подобрано неправильно или проведено слишком поздно и оказалось неэффективным, то развивается терминальная стадия ОПН с высокой вероятностью летального исхода. Для нее характерно:
- одышка, кашель, обусловленные скоплением жидкости в легких;
- выделение мокроты с примесью крови;
- подкожные кровоизлияния и внутренние кровотечения;
- потеря сознания, кома;
- спазмы и судороги мышц;
- тяжелые нарушения сердечного ритма.
Совет: При обнаружении даже незначительного снижения диуреза, особенно если присутствуют заболевания почек или другие патологии, необходимо сразу обратиться к нефрологу. Такие нарушения могут быть началом развития ОПН.
Диагностика ОПН
При острой почечной недостаточности диагностика заболевания проводится с применением как лабораторных, так и инструментальных методов. В лабораторных анализах присутствуют следующие отклонения от нормы:
- общий анализ крови характеризуется снижением уровня гемоглобина, повышением концентрации лейкоцитов, увеличением СОЭ;
- в общем анализе мочи обнаруживается белок, цилиндры, снижение плотности, повышенное содержание эритроцитов и лейкоцитов, снижение уровня тромбоцитов;
- суточный анализ мочи характеризуется значительным снижением диуреза;
- в биохимическом анализе крови обнаруживается повышенный уровень креатинина и мочевины, а также повышение концентрации калия и снижение концентрации натрия и кальция.
Из инструментальных методов диагностики применяется:
- ЭКГ, используют для контроля работы сердца, которая может быть нарушена в связи с гиперкалиемией;
- УЗИ, позволяет оценить размеры почек, уровень кровоснабжения и наличие обструкции;
- биопсия почки;
- рентгенография легких и сердца.
Лечение и неотложная помощь при ОПН
При острой почечной недостаточности неотложная помощь заключается в быстрой доставке человека в стационар больницы. При этом пациенту нужно обеспечить состояние покоя, тепло и горизонтальное положение тела. Лучше всего вызвать скорую помощь, так как в этом случае квалифицированные врачи смогут прямо на место принять все необходимые меры.
При острой почечной недостаточности лечение проводится с учетом стадии заболевания и причины его вызвавшей. После устранения этиологического фактора, необходимо провести восстановление гомеостаза и выделительной функции почек. С учетом причины ОПН может понадобиться:
- прием антибиотиков при инфекционных заболеваниях;
- восполнение объема жидкости (при снижении объема циркулирующей крови);
- применение мочегонных средств и ограничение жидкости для снижения отеков и увеличения выработки мочи;
- прием сердечных препаратов при нарушении работы сердца;
- прием препаратов для снижения артериального давления в случае его повышения;
- оперативное вмешательство для восстановления поврежденных в результате травмы тканей почки или для удаления препятствий, мешающих оттоку мочи;
- прием препаратов для улучшения кровоснабжения и кровотока в нефронах;
- дезинтоксикация организма в случае отравлений (промывание желудка, введение антидотов и др.).
Для выведения из крови токсических продуктов применяют гемодиализ, плазмаферез, перитонеальный диализ, гемосорбцию. Кислотно-основной и водно-электролитный баланс восстанавливают при помощи введения солевых растворов калия, натрия, кальция и др. Эти процедуры используются временно, пока не восстановится почечная функция. При своевременном лечении ОПН имеет благоприятный прогноз.
>
Но возможно правильнее лечить не следствие, а причину?
Вконтакте
Острая почечная недостаточность (ОПН) представляет собой внезапное нарушение функций обеих почек, вызванное снижением почечного кровотока и замедлением процессов клубочковой фильтрации и канальцевой реабсорбции. В результате происходит задержка или полное прекращение выведения из организма токсических веществ и расстройство кислотно-основного, электролитного и водного баланса.
При правильном и своевременном лечении эти патологические изменения являются обратимыми. По данным медицинской статистики ежегодно случаи ОПН регистрируются примерно у 200 человек на 1 миллион.
Формы и причины ОПН
В зависимости от того, какие процессы привели к возникновению острой почечной недостаточности, выделяют преренальную, ренальную и постренальную формы.
Преренальная форма ОПН
Преренальная форма ОПН характеризуется значительным сокращением почечного кровотока и снижением скорости клубочковой фильтрации. Такие нарушения в работе почек связаны с общим уменьшением объема циркулирующей крови в организме. В случае если нормальное кровоснабжение органа не будет восстановлено в кратчайшие сроки, возможны ишемия или некроз почечной ткани. Основными причинами развития преренальной ОПН являются:
- снижение сердечного выброса;
- тромбоэмболия легочной артерии;
- операции и травмы, сопровождающиеся значительной кровопотерей;
- обширные ожоги;
- обезвоживание, вызванное диареей, рвотой;
- прием мочегонных препаратов;
- внезапное снижение сосудистого тонуса.
Ренальная форма ОПН
При ренальной форме ОПН наблюдается поражение паренхимы почек. Оно может быть вызвано воспалительными процессами, токсическим действием или патологиями сосудов почек, которые приводят к недостаточности кровоснабжения органа. Ренальная ОПН является следствием некроза эпителиальных клеток канальцев почек. В результате происходит нарушение целостности канальцев и выход их содержимого в окружающие ткани почки. К развитию ренальной формы ОПН могут приводить следующие факторы:
- интоксикация различными ядами, лекарствами, рентгеноконтрастными соединениями, тяжелыми металлами, укусами змей или насекомых и др.;
- заболевания почек: интерстициальный нефрит, острый пиелонефрит и гломерулонефрит;
- поражение почечных сосудов (тромбоз, аневризма, атеросклероз, васкулит и др.);
- травмы почек.

Антибиотики, сульфаниламиды, аминогликозиды, противоопухолевые средства, оказывают токсическое действие на почки
Важно: Длительный прием лекарственных средств, оказывающих нефротоксическое действие, без предварительной консультации с врачом может стать причиной ОПН.
Постренальная ОПН
Постренальная ОПН развивается в результате острого нарушения пассажа мочи. При этой форме ОПН функция почек сохраняется, но процесс выделения мочи затруднен. Возможно возникновение ишемии почечной ткани, так как переполненные мочой лоханки начинают сдавливать окружающие ткани почки. К причинам возникновения постренальной ОПН относятся:
- спазм сфинктера мочевого пузыря;
- закупорка мочеточников вследствие мочекаменной болезни;
- опухоли мочевого пузыря, предстательной железы, мочевыводящих каналов, органов таза;
- травмы и гематомы;
- воспалительные заболевания мочеточников или мочевого пузыря.
Стадии и симптомы ОПН
Характерные симптомы ОПН развиваются очень быстро. Отмечается резкое ухудшение общего состояния пациента и нарушение почечной функции. В клинической картине острой почечной недостаточности выделяют стадии, для каждой из которых характерны определенные признаки:
- начальная стадия;
- стадия олигоанурии;
- стадия полиурии;
- стадия выздоровления.
На первой стадии ОПН симптомы определяются причиной заболевания. Это могут быть признаки интоксикации, шока или проявления какого-то заболевания. Так, при инфекционном поражении почек отмечается лихорадка, головная боль, мышечная слабость. В случае кишечной инфекции присутствует рвота и диарея. Для токсического поражения почек характерны проявления желтухи, анемия, возможны судороги. Если причиной ОПН является острый гломерулонефрит, то отмечается выделение мочи с примесью крови и боли в области поясницы. Для первой стадии ОПН характерно снижение артериального давления, бледность, учащенный пульс, незначительное уменьшение диуреза (до 10%).
Стадия олигоанурии при ОПН является самой тяжелой и представляет наибольшую опасность для жизни пациента. Она характеризуется следующими симптомами:
- резкое снижение или прекращение выделения мочи;
- интоксикация продуктами азотистого обмена, проявляющаяся в виде тошноты, рвоты, зуда кожных покровов, учащения дыхания, потери аппетита, тахикардии;
- повышение артериального давления;
- спутанность и потеря сознания, коматозное состояние;
- отеки подкожной клетчатки, внутренних органов и полостей;
- повышение массы тела за счет наличия избытка жидкости в организме;
- общее тяжелое состояние.
Дальнейшее течение ОПН определяется успешностью проведенной терапии на второй стадии. При благоприятном исходе наступает стадия полиурии и последующего выздоровления. Сначала наблюдается постепенное увеличение диуреза, а затем развивается полиурия. Из организма выводится избыточная жидкость, уменьшаются отеки, кровь очищается от токсических продуктов. Стадия полиурии может быть опасна возникновением обезвоживания и нарушениями электролитного баланса (например, гипокалиемией). Примерно через месяц диурез приходит в норму и начинается период выздоровления, который может длиться до 1 года.
Если лечение было подобрано неправильно или проведено слишком поздно и оказалось неэффективным, то развивается терминальная стадия ОПН с высокой вероятностью летального исхода. Для нее характерно:
- одышка, кашель, обусловленные скоплением жидкости в легких;
- выделение мокроты с примесью крови;
- подкожные кровоизлияния и внутренние кровотечения;
- потеря сознания, кома;
- спазмы и судороги мышц;
- тяжелые нарушения сердечного ритма.
Совет: При обнаружении даже незначительного снижения диуреза, особенно если присутствуют заболевания почек или другие патологии, необходимо сразу обратиться к нефрологу. Такие нарушения могут быть началом развития ОПН.
Диагностика ОПН
При острой почечной недостаточности диагностика заболевания проводится с применением как лабораторных, так и инструментальных методов. В лабораторных анализах присутствуют следующие отклонения от нормы:
- общий анализ крови характеризуется снижением уровня гемоглобина, повышением концентрации лейкоцитов, увеличением СОЭ;
- в общем анализе мочи обнаруживается белок, цилиндры, снижение плотности, повышенное содержание эритроцитов и лейкоцитов, снижение уровня тромбоцитов;
- суточный анализ мочи характеризуется значительным снижением диуреза;
- в биохимическом анализе крови обнаруживается повышенный уровень креатинина и мочевины, а также повышение концентрации калия и снижение концентрации натрия и кальция.

Анализ мочи позволяет обнаружить нарушения функции почек
Из инструментальных методов диагностики применяется:
- ЭКГ, используют для контроля работы сердца, которая может быть нарушена в связи с гиперкалиемией;
- УЗИ, позволяет оценить размеры почек, уровень кровоснабжения и наличие обструкции;
- биопсия почки;
- рентгенография легких и сердца.
Лечение и неотложная помощь при ОПН
При острой почечной недостаточности неотложная помощь заключается в быстрой доставке человека в стационар больницы. При этом пациенту нужно обеспечить состояние покоя, тепло и горизонтальное положение тела. Лучше всего вызвать скорую помощь, так как в этом случае квалифицированные врачи смогут прямо на место принять все необходимые меры.

При тяжелом состоянии в случае ОПН больного необходимо доставить в больницу
При острой почечной недостаточности лечение проводится с учетом стадии заболевания и причины его вызвавшей. После устранения этиологического фактора, необходимо провести восстановление гомеостаза и выделительной функции почек. С учетом причины ОПН может понадобиться:
- прием антибиотиков при инфекционных заболеваниях;
- восполнение объема жидкости (при снижении объема циркулирующей крови);
- применение мочегонных средств и ограничение жидкости для снижения отеков и увеличения выработки мочи;
- прием сердечных препаратов при нарушении работы сердца;
- прием препаратов для снижения артериального давления в случае его повышения;
- оперативное вмешательство для восстановления поврежденных в результате травмы тканей почки или для удаления препятствий, мешающих оттоку мочи;
- прием препаратов для улучшения кровоснабжения и кровотока в нефронах;
- дезинтоксикация организма в случае отравлений (промывание желудка, введение антидотов и др.).
Для выведения из крови токсических продуктов применяют гемодиализ, плазмаферез, перитонеальный диализ, гемосорбцию. Кислотно-основной и водно-электролитный баланс восстанавливают при помощи введения солевых растворов калия, натрия, кальция и др. Эти процедуры используются временно, пока не восстановится почечная функция. При своевременном лечении ОПН имеет благоприятный прогноз.
Современные методы лечения острой почечной недостаточности
Современные методы лечения ОПН
Острая почечная недостаточность (ОПН)
Острая почечная недостаточность (ОПН) - это клинико-биохимический синдром, характеризующийся быстрым снижением преимущественно экскреторной функции почек (в течение часов или дней), что клинически проявляется уменьшением скорости клубочковой фильтрации, увеличением содержания в крови азотистых метаболитов, изменениями объема внеклеточной жидкости, расстройствами кислотно основного и электролитного гомеостаза.
Классификация.
В зависимости от причин и механизмов развития рассматривают преренальную, ренальную и постренальную ОПН.
Кроме того, ОПН нередко разделяют на олигурическую и неолигурическую, а в течении олигурической ОПН выделяют четыре периода: период начальных проявлений (клинической картины ОПН как таковой нет, клини- ка определяется тем состоянием, которое приводит к ОПН), период анурииолигурии, период полиуирии, период выздоровления.
Однако такую четкую периодизацию обычно можно наблюдать только при остром тубулярном некрозе (ОТН).
Этиология. Доминирует ОТН - 45%; преренальные случаи составляют 21%; ОПН, развивающаяся на фоне существующей ХПН («ОПН на ХПН») - 13%; обструкция мочевыводящих путей - 10%; паренхиматозные заболевания почек- 4,5%; ОТИН- 1,6%. Доля сосудистой патологии составляет только 1%.
Причины преренальной ОПН:
- состояния, связанные с уменьшением внеклеточного объема жидкости (ВОЖ);
- гиповолемия (почечные потери жидкости - диуретики, осмотический диурез при СД, надпочечниковая недостаточность; потери через ЖКТ и кожу, а также кровопотери любой этиологии; перераспределение жидкости в брюшную полость при гепатопатии, НС, гипоальбуминемии другой этиологии, кишечная непроходимость, панкреатит, перитонит);
- снижение сердечного выброса (выраженная СН, кардиогенный шок, поражения клапанов сердца, патология миокарда, аритмии, ТЭЛА, тампонада перикарда и пр.);
- нарушение соотношения между системным и почечным сосудистым сопротивлением при артериальной гипотензии, сепсисе, гипоксемии, анафилаксии, лечении ИЛ 2 и ИФН, синдроме гиперстимуляции яичников; почечной вазоконс трикции, блокаде синтеза простагландинов, гиперкальциемии;
- гипоперфузия почек вследствие нарушения почечной сосудистой аугорегуляции в связи с избыточной дилатацией выносящей артериолы при применении иАПФ, блокаторов ATj рецепторов ангиотензина II (А II); - синдром повышенной вязкости крови (ми елома, макроглобулинемия, полицитемия).
Причины ренальной ОПН:
- острый тубулярный некроз при нарушении гемодинамики (сердечно сосудистые операции, сепсис), токсическом воздействии антибиотиков, йодсодержащих рентгеноконтрастных препаратов, анестетиков, иммуносупрессантов и цитостатиков, ртутьсодержащих препаратов, змеиного яда;
- миоглобиновый рабдомиолиз: мышечная травма, инфекции, полимиозит, метаболические нарушения, гиперосмолярная кома, диабетический кетоадидоз, выраженная гиперкалиемия, гипернатриемия, гипонатриемия, гипофосфатемия, гипертиреоз, высокая гипертермия, воздействие этиленгликоля, СО, хлорида ртути, прием лекарств (фибраты, статины, опиоиды, амфетамин), врожденные болезни (мышечные дистрофии, дефицит карнитина, болезнь Мак Ардля);
- гемолиз и гемоглобинурия: малярия, механическая деструкция эритроцитов при экстракорпоральных циркуляциях или металлических протезах, посттрансфузионные реакции, гемолиз другой этиологии, тепловой удар, ожоги, дефицит глюкозо-6-фосфатдегидрогеназы и другие эритроцитарные ферментопатии, синдром Маркиафавы-Микели, влияние органических веществ (анилин, фенол, хинин, глицерол, бензол, фенол, гидралазин), ядов насекомых;
- острый тубулоинтерстициальный нефрит: аллергический (при приеме р-лактамов, триметоприма, сульфаниламидов, ингибиторов циклооксигеназы, диуретиков, каптоприла, рифампицина); инфекционный (бактериальный - острый пиелонефрит, лептоспироз и др.; вирусный, грибковый); при лейкозах, лимфомах, саркоидозе; идиопатический;
- нарушения проходимости сосудов (билатеральный стеноз почечной артерии вследствие тромбоза/эмболии, тромбоз почечных вен; атероэмболия, тромботическая микроангиопатия, гемолитико уремический синдром, тромботическая тромбоцитопеническая пурпура, послеродовый тромбоз, АФС, ДВС, склеродермия, ЗАГ, пострадиационные поражения, васкулиты);
- гломерулопатии: ОГН, БПГН (АНЦА-ассоциированные васкулиты, малоиммунный ГН), IgA нефропатия, МзПГН, люпус нефрит, болезнь Шенлейн-Геноха, смешанная криоглобу линемия, болезнь Гудпасчера;
- кортикальный некроз, abruptio placentae, септический аборт, ДВС.
Причины постренальной ОПН:
- обструкция мочеточников: мочекаменная болезнь, тромбы, папиллярный некроз, опухоли, сдавление извне (опухоли, ретроперитонеальный фиброз), уретероцеле, ятрогенная перевязка мочеточника;
- обструкция мочевого пузыря: нейрогенный мочевой пузырь, доброкачественная гиперплазия простаты, мочекаменная болезнь, тромбы, опухоли, дивертикулез мочевого пузыря;
- обструкция уретры: фимоз, стриктура уретры, врожденные уретральные клапаны.
Клиническая картина.
Клинически ОПН может проявляться в виде нескольких вариантов:
1. Латентный (неолигурическая ОПН) - характеризуется только лабораторными изменениями (азотемия и снижение СКФ), но объем мочи у пациентов не уменьшается.
Содержание креатинина (Сгр) и азот мочевины (Ur) в сыворотке крови традиционно являются наиболее доступными в клинической практике показателями, являющимися маркерами снижения СКФ и, таким образом, позволяющими оценивать функциональное состояние почек.
Более надежно с уровнем СКФ коррелирует Сгр. Однако следует помнить, что повышение Сгр не всегда связано с развитием ПН.
Это касается случаев массивного поступления креатинина из поврежденной поперечно полосатой мускулатуры при различных вариантах рабдо миолиза и блокады его канальцевой секреции триметопримом и циметидином. В большинстве случаев концентрации креатинина и мочевины в крови нарастают по мере падения СКФ, пропорционально, приблизительно в соотношении 1:60 (в ммоль/л).
Непропорциональное повышение мочевины в сыворотке крови может наблюдаться при снижении тока мочи в дистальном отделе нефрона в случаях преренальной ОПН или постренальной обструкции мочевыводящих путей. Кроме того, повышению концентрации креатинина могут способствовать лихорадка, применение ГКС и тетрациклина, а также избыточное потребление белка.
Неолигурическими являются от 20-30% до половины случаев ОПН.
Неолигурический вариант чаше бывает при применении аминогликозидов и рентгеноконтрастируюших препаратов, хотя может развиваться при остром снижении почечной функции любой этиологии.
Неолигурическая ОПН имеет более благоприятное течение и прогноз, поскольку связана с менее выраженными морфологическими и функциональными изменениями почечной ткани.
У этих больных СКФ в 2-3 раза выше, меньше выраженность азотемии по сравнению с олигурическими больными.
Естественно, что потребность в ЗПТ у неолигурических больных значительно ниже.
2. Олиго- и анурия.
Олигурия - снижение объема суточной мочи менее 400 мл.
Развитие олигурии свидетельствует либо о выключении из работы большинства клубочков, либо о крайне выраженном снижении СКФ в каждом из них.
Анурию определяют при снижении диуреза менее 50 мл/сут.
Развитие этого симптома чаще всего бывает связано с полной обструкцией мочевыводящих путей, а также с быстропрогрессирующим гломерулонефритом, кортикальным некрозом и инфарктами почек. Чередование олигурии и полиурии позволяет предполагать частичную мочевую обструкцию.
3. Преобладание клинической симптоматики основного заболевания, вызвавшей ОПН. Полиэтиологичность ОПН предполагает наличие симптомов вызвавшего данное состояние заболевания помимо клинических признаков снижения функции почек.
4. Развернутая ПН (уремия, анемия, дизэлектролитемия, метаболический ацидоз). Тяжесть клинической симптоматики уремического синдрома и связанных с ним состояний, отражающих нарушение парциальных функций почек, зависит от времени выявления ОПН, быстроты ее развития, вызвавшей причины и резидуальной функции. Обычно выраженные азотемия и уремия отражают факт несвоевременной диагностики ОПН и связаны с неблагопрятным прогнозом.
Уремические симптомы включают: появление кожного зуда, тошноты, рвоты, нарушений ЦНС, вплоть до коматозного состояния, развития плеврита и перикардита. Уремия, как правило, сопровождается развитием малокровия, метаболическим ацидозом, электролитными нарушеня ми (гиперкалиемией, гиперфосфатемией, чаще умеренной гипокальциемией и гипонатриемией, реже гиперкальциемией и гипернатриемией), гипергидратацией (особенно при снижении диуреза).
Однако эти осложнения в том или ином сочетании могут быть и при других клинических вариантах ОПН. Каждое из этих состояний требует наблюдения и своевременной коррекции.
Диагностика.
В диагностике ОПН важно соблюдать несколько принципов - своевременность, неотложность и последовательность, что имеет важное практическое значение.
Ранняя диагностика любого варианта ОПН позволяет начать своевременное консервативное лечение, предотвратить развитие выраженной уремии и ее осложнений, необходимость проведения ЗПТ, предотвратить или уменьшить повреждение почечной ткани и улучшить ближайший и отдаленный прогноз. Поэтому при наблюдении за больным, относящимся к группам риска, следует регулярно проводить скрин нинговые исследования в отношении показателей функционального состояния почек - контроль диуреза, анализов мочи, определение Сгр и мочевины в сыворотке крови, параметров КОС крови, УЗИ почек.
В практической работе каждый случай ОПН требует максимально быстрого определения типа ОПН, его этиологии.
Нужно иметь в виду, что несвоевременная диагностика преренальной ОПН чревата формированием ренальной.
Ранняя диагностика постренальной ОПН позволяет вовремя минимизировать обструкцию мочевыводящих путей оперативными методами.
Основные этапы диагностики ОПН при выявлении снижения СКФ и/или азотемии:
1. Подтверждение азотемии, снижения СКФ, т. е. ПН.
2. Дифференциальная диагностика ОПН и ХПН.
3. Проведение дифференциальной диагностики пре- и постренальной ОПН.
При определении преренальной ОПН максимально быстро осуществить коррекцию гиповолемии, системной гемодинамики. В случае выявления постренальной ОПН устранить обструкцию мочевыводящих путей.
4. При исключении пре и постренальной ОПН уточнить этиологию ренальной ОПН (патология почечных сосудов, тубулярный некроз, кортикальный некроз, ОТИН, гломерулопатия).
На каждом этапе диагностики необходимо решение вопроса о показаниях к заместительной почечной терапии (ЗПТ).
Диагностика преренальной ОПН
Преренальную азотемию в первую очередь следует подозревать при наличии состояний, способных привести к гиповолемии и соответствующей клинической симптоматике.
Большое значение на этом этапе имеет правильная интерпретация анализов мочи. Нормальные анализы или незначительные изменения в первую очередь позволяют предполагать наличие преренальной ОПН, в то время как протеинурия, изменения клеточного состава мочи, цилиндру рия заставляют думать об истинной почечной патологии.
На данном этапе диагностики целесообразно определение почечных индексов, которые могут оказать существенную помощь в разграничении вариантов ОПН, и в первую очередь преренальной ОПН и ОТН.
У большинства пациентов с преренальной ОПН увеличено соотношение Ur/Cr в сыворотке крови более 60:1. Показатели фракционной экскреции натрия (EF Na) и концентрация натрия в моче (U Na) снижены соответственно < 1 % и < 20 ммоль/л.
Показатель EF Na обладает достаточными чувствительностью и специфичностью для диагностики преренальной ОПН.
Однако следует помнить, что пониженная EF Na может быть и в случаях ОТН при иммунных гломерулопатиях, в начальных стадиях (первые часы) обструкции мочевыводя щих путей, при ОТН, осложняющем применение рентгеноконтрастирующих препаратов.
У пятой части больных с ОТН и неолигурической формой ОПН экскретируемая фракция натрия также остается низкой (< 1%).
Величина EF Na будет повышена при развитии преренальной ОПН на фоне предсуществующей ХПН или при применении петлевых диуретиков.
В этих случаях окончательный диагноз ОПН устанавливают ex juvantibus (значительное улучшение показателей азотовыделительной функции почек после коррекции гиповолемии).
У больных с ХПН адаптационные возможности почек к развившейся гиповолемии снижены вследствие выраженных тубулоинтерстициальных изменений.
Наконец, EF Na у больных с преренальной ОПН может нарастать в ситуациях осмотического диуреза, например при диабетическом кетоацидозе или внутривенном введении глюкозы.
В этих случаях более существенную диагностическую информацию может дать определение концентрации хлора в моче (U Q).
Таким образом, у значительной доли пациентов на этапе диагностики преренальной ОПН можно выявить симптомы абсолютной или относительной гиповолемии и, соответственно, установить предварительный диагноз.
В этом случае необходимо немедленно начать консервативное лечение, направленное на коррекцию ОЦК, стабилизацию АД, увеличение сердечного выброса (СВ).
Своевременное начало терапии, с одной стороны, имеет диагностическое значение, поскольку быстрое восстановление диуреза и снижение азотемии на фоне указанного лечения, несомненно, свидетельствует в пользу преренальной ОПН.
С другой стороны, восстановление или улучшение почечной перфузии снижает риск ише мических изменений в почечной ткани и может предотвратить развитие ОТН.
Диагностика вариантов ренальной ОПН
Основные варианты истинной ренальной ОПН.
Острый тубулярный некроз.
Преренальная ОПН и ишемический ОТН имеют общие механизмы развития и считаются разными стадиями одного и того же процесса.
Ишемический ОТН следует предполагать при наличии признаков нарушения системной гемодинамики и гиповолемии. В отличие от преренальной ОПН в случае более глубокой ишемии ткани почек или при ее более длительной экспозиции, ведущей к развитию некроза канальцев, после коррекции системной гемодинамики улучшения показателей функционального состояния почек не происходит.
Развитие ОТН может быть связано с повреждением канальцев экзогенными и эндогенными нефротоксическими воздействиями. Наиболее частыми причинами последних яатяются лекарственные средства.
В диагностике данного варианта ОПН имеет значение определение связи между развитием ОПН, временем приема препарата, длительностью, суммарной дозой и достижением критической концентрации в крови. Острый тубулоинтерстициальный нефрит.
Этот вариант ренальной ОПН в подавляющем большинстве случаев возникает на фоне применения целого ряда лекарств.
Течение болезни зачастую сопровождается системными симптомами аллергии - гипертермией, артралгиями, эритемой.
Лабораторные данные указывают на эозинофилию в крови.
Важным признаком ОТИН лекарственной этиологии является повышение содержания эозинофилов в моче.
Следует отметить, что с лекарственными поражениями почек также связано развитие ОТН, тактика лечения которого отличается от терапии ОТИН лекарственной этиологии.
Поэтому в случае отсутствия возможности провести дифференциальную диагностику между этими состояниями целесообразно проведение морфологического исследования почечной ткани.
Таким образом, биопсия почки показана в любых случаях ренальной ОПН с невыясненной окончательно этиологией.
Диагностика ОТИН также должна быть связана с поиском других этиологических факторов - инфекций, болезней крови, СКВ, отторжения почечного трансплантата у больных с пересаженной почкой. Гломерулопатии как причина ОПН.
Целый ряд заболеваний почечных клубочков может приводить к развитию ОПН.
Подозрение на эту форму ОПН должно возникать при обнаружении изменений, характерных для патологии клубочков. Обследование таких больных должно включать целый ряд параметров, позволяющих уточнить конкретное заболевание, которое является непосредственным виновником гломерулярного поражения. При васкулитах с гломерулопатиями необходимо исследовать антинуклеарный фактор, АНЦА, AT к ГБМ, LE клетки, посев крови, комплемент, криоглобулины, ревматоидный фактор, форму 50, HbsAg, анти HCV.
При плазмоклеточных дискразиях - легкие цепи иммуноглобулинов, белок Бена-Джонса, протеинограмма.
При установлении диагноза ОПН на фоне гломерулярных болезней или васкулита для окончательной диагностики необходимо проведение срочной биопсии почек, показаниями к которой при ОПН являются: постепенное начало, отсутствие явной внешней причины, протеинурия более 1 г/сут, гематурия, системность клинических проявлений, длительный период олигурии/анурии (10-14 дней).
В данном случае морфологическое исследование почечной ткани необходимо в первую очередь, для исключения вариантов БПГН.
Своевременная диагностика и иммуносупрессивная терапия этой почечной патологии позволяет существенно отдалить развитие ХПН.
При обоснованном подозрении на БПГН и при отсутствии возможности выполнения морфологического исследования или противопоказаниях к проведению биопсии почки может быть назначена эмпирическая иммуносупрессивная терапия.
Окклюзия сосудов почек.
Диагностика билатеральной окклюзии крупных сосудов почек (артерий и вен) требует включения в программу обследования больного с ОПН допплерографии сосудов почек как скриннингового метода.
Окончательный диагноз устанавливается после ангиографии.
Болезни мелких сосудов, способных привести к ОПН (см. этиологию), требуют проведения соответствующей диагностики, которая описана в соответствующих разделах сайта и многочисленных руководствах.
Кортикальный некроз обусловлен тяжелым поражением клубочков и канальцев.
Развивается он редко и связан главным образом с акушерской патологией - отслойкой плаценты.
Данное состояние также может осложнять течение сепсиса и ДВС синдрома.
Заподозрить кортикальный некроз можно при развитии стойкой анурии. Подтверждение в остром периоде можно получить только при морфологическом исследовании.
Клинически диагноз можно установить ретроспективно, в случае отсутствия разрешения предполагаемого
ОТН в течение 1-1,5 мес.
Диагностика постренальной ОПН.
Подозрение на обструкцию мочевыводяших путей должно возникать при наличии никтурии, конкрементов, признаков ИМП, опухолей мочевого пузыря, простаты, образований брюшной полости, симптомов почечной колики, болей в надлобковой области.
Для скриннингового выявления возможной обструкции мочевыводящих путей с развитием ОПН в большинстве случаев бывает достаточно УЗИ почек и мочевого пузыря.
При отсутствии типичных признаков расширения чашечно ло ханочной системы в случаях, подозрительных на постренальную ОПН, необходимо выполнить повторное УЗИ почек через 24 ч.
В каждом конкретном случае, особенно при подозрении на обструктивную ОПН на фоне онкологической патологии, полезную информацию о состоянии мочевыводящих путей могут дать компьютерная томография или магнитно резонансная томография. Применение радиологических методов для выя вления обструкции (динамическая сцинтиграфия) оправдано при относительной сохранности почечного кровотока, в чем можно убедиться с помощью допплерографии почек.
Методы диагностики с парентеральным введением рентгено контрастных препаратов использоваться не должны, поскольку они могут оказать дополнительное нефротоксическое воздействие.
Следует подчеркнуть, что при сохраняющейся неопределенности в отношении обструкции мочевыводящих путей и необходимости дополнительных исследований диагностика и исключение других вариантов ОПН не должны быть приостановлены.
Лечение.
Терапия преренальной ОПН зависит от вызвавшей ОПН причины - гиповолемии, низкого СВ, снижения периферического сосудистого сопротивления.
Коррекция уменьшения ОЦК. Изотонический раствор NaCl является средством выбора для большинства пациентов со значимой гиповолемией, приведшей к развитию преренальной ОПН.
Однако большие объемы вводимого в/в NaCl могут приводить к развитию гиперхлоремического метаболического ацидоза, особенно у больных с сохранным диурезом и дефекацией (за счет потери бикарбоната).
Поэтому при склонности к гиперхлоремическому метаболическому ацидозу инфузионную терапию следует начинать с раствора Рингера лактата, поскольку сам лактат метаболизируется в печени в бикарбонат и позволяет контролировать развитие/прогрессирование ацидоза.
Другой альтернативой физиологическому раствору может быть гипотонический раствор NaCl с добавлением бикарбоната (например, 0,25-0,45% NaCl + 50-100 мэкв бикарбоната натрия).
В условиях незначительного дефицита ОЦК и при развитии гипернатриемии следует применять гипотонический раствор NaCl.
Гипертонические растворы NaCl используют при ОПН на фоне травматического повреждения или ожогов, поскольку небольшие объемы этого препарата могут вызывать значительное увеличение ОЦК за счет активного перемещения воды из внеклеточного во внутрисосудистое пространство. Следует подчеркнуть, что, в отличие от кристаллоидов коллоидные растворы, включая гидрок сиэтилкрахмала (HES), декстраны и желатины, при преренальной ОПН использовать не рекомендуется.
Несмотря на их эффективность в лечении гиповолемии, сопутствующее значительное нарастание коллоидно осмотического (онкотического) давления крови может привести к дальнейшему падению СКФ.
В случае развития пре ОПН на фоне острого геморрагического шока лечение гиповолемии, естественно, следует начинать с введения препаратов крови. Если последние недоступны, терапия первого шага - введение кристаллоидов (изотонический раствор NaCl), а при отсутствии эффекта в отношении системной гемодинамики небелковые коллоидные растворы и альбумин.
При преренальной ОПН на фоне гипоальбу минемии и перераспределении объемов в третьи пространства (полости, подкожную клетчатку) показаны мероприятия, ведущие к повышению эффективного артериального объема крови - погружение тела в воду и в/в введение альбумина.
Выраженные периферические и полостные отеки при гипоальбуминемии часто резистентны к лечению диуретиками. Кроме того, изолированное применение диуретиков у этих больных может вызвать нарастание гиповолемии и азотемии.
Временный эффект можно получить при комбинированном применении фуросемида и альбумина в дозе 50 г/сут.
Дозы фуросемида могут варьировать от 40 до 1000 мг/сут. Применение альбумина существенно улучшает диуретический эффект мочегонных, приводит к увеличению диуреза, снижению массы тела и, что весьма важно, к снижению или разрешению преренальной азотемии.
Около 90% вводимого фуросемида связывается с альбумином, поэтому при гипоальбуминемии изменяется распределение мочегонного в сосудистом и внесосудистом пространстве.
Добавление к лечению альбумина помимо временного увеличения онкотического давления плазмы крови и привлечения жидкости из интерстиин альных пространств приводит к увеличению доставки фуросемида к его рецепторам в толстом восходящем отделе петли Генле. Так, у пациентов с гипоальбуминемией при монотерапии содержание фуросемида в моче составляло 7-12% от введенной дозы.
Комбинированная терапия фуросемидом и альбумином увеличивает мочевую экскрецию первого до 24-30% .
Коррекция низкого сердечного выброса.
Лечение должно быть направлено на увеличение СВ и снижение постнагрузки. Тактика увеличения СВ заключается в снижении увеличенного внеклеточного объема с помощью диуретиков или ультрафильтрации (УФ); улучшении работы сердца применением инотроп ных препаратов или (и) периферических вазодилататоров.
Применение диуретиков (в частности, фуросемида) приводит к снижению конечного диастолического объема левого желудочка и улучшению субэндокардиальной перфузии.
Кроме того, на фоне терапии фуросемидом сократительная функция сердца улучшается в процессе снижения давления заклинивания легочных капилляров.
Теоретически лечение петлевыми диуретиками может привести к критическому снижению наполнения ЛЖ и падению СВ.
Поэтому введение диуретиков должно происходить под тщательным контролем водного баланса, ЦВД.
Часть больных с выраженной СН и ОПН имеют весьма низкий CB высокий уровень эндогенных вазопрессоров и практически резистентны к терапии мочегонными, инотропными агентами и вазодилататорами.
В этом случае существенный эффект может дать аппаратная ультрафильтрация (УФ), применение которой приводит к увеличению диуреза и улучшению ответа на медикаментозную терапию и снижению уровня прессорных факторов в циркуляции.
Другие болезни с эу или гиперволемией на фоне низкого СВ, способные привести к развитию пре ОПН, - ИМ, перикардиальная тампонада, массивная эмболия легочной артерии.
В этих случаях разрешение преренальной азотемии зависит, в первую очередь от лечения основного процесса.
Коррекция состояний с пониженным периферическим сосудистым сопротивлением.
Используется изотонический раствор NaCl.
Эффективность применения небелковых коллоидных растворов и альбумина не доказана.
Преренальная азотемия зачастую случается у больных с циррозами и другими заболеваниями печени, осложняющимися печеночной недостаточностью и асцитом.
Этим больным показано ограничение приема NaCl.
Мочегонные эффективны в отношении разрешения асцита у 73% больных. Однако стимуляция диуреза (фуросемид + спиронолактон) может приводить к ухудшению функционального состояния почек.
В этом случае лечением выбора является инфузия альбумина в дозе 40 г в/в вместе с парацентезом (4-6 л за сеанс).
Парацентез с введением альбумина позволяет существенно сократить сроки госпитализации.
Поэтому сочетание парацентеза и альбумина следует использовать в качестве начальной терапии случаев печеночной недостаточности, выраженного асцита (и при наличии, и при отсутствии преренальной азотемии); поддерживающую терапию следует проводить мочегонными.
Для предотвращения ухудшения функции почек при проведении парацентеза у больных с выраженным асцитом показано введение декстрана (декстран 70).
Целесообразность применения допамина для вазодилатации почечного артериального ложа при преренальной ОПН в настоящее время не доказана.
Лечение ренальной ОПН.
ОПН ишемической и нефротоксической этиологии.
Коррекцию ОЦК и водно электролитных нарушений следует проводить солевыми растворами, поскольку есть экспериментальные данные об уменьшении тяжести ОТН на фоне предварительной нагрузки хлоридом натрия.
Принципы применения кристаллоидов аналогичны таковым при лечении преренальной ОПН (см. ниже).
Несомненную значимость в профилактике ОТН имеет осторожность в выборе диагностических процедур и лекарственных препаратов, обладающих потенциальной нефротоксичностью, мониторирование состояния больного, особенно относящегося к группам риска и своевременная коррекция нарушений системной и регионарной гемодинамики.
Традиционные методы медикаментозной профилактики касались применения осмотических и петлевых диуретиков, а также допамина.
Ранее считали, что диуретики за счет увеличения диуреза могут предотвратить обструкцию канальцев, которая отчасти связана со снижением СКФ при ОТН. В дальнейшем, однако, было продемонстрировано, что и петлевые диуретики, и маннитол не обладают профилактическими свойствами в отношении развития ОТН и никак не влияют на прогноз развернутого ОТН.
Вместе с тем применение мочегонных может трансформировать олигурические варианты ОТН в неолигурические и, таким образом, снижать потребность в ЗПТ.
С этой целью используют маннитол в низких дозах (15-25 г), болюсное или капельное введение фуросемида, которые эффективны только на ранних стадиях ОТН.
При отсутствии увеличения диуреза после терапии данными диуретиками в дальнейшем продолжать их введение и наращивать дозы не следует.
Это может привести к нежелательным последствиям - гиперосмолярной коме, панкреатиту, глухоте.
Кроме того, при введении маннитола в больших дозах у лиц со сниженным диурезом высок риск развития отека легких.
Результаты последних разработок, в том числе и данные метанализов, подтвердили, что применение фуросемида у пациентов с наличием ОПН или высоким риском ее развития не оказывает сушественного влияния на внутрибольничную летальность, необходимость последующего назначения ЗПТ, числа последующих сеансов гемодиализа и количества пациентов со стойкой олигурией.
В то же время высокие дозы этого петлевого диуретика, которые обычно применяются у пациентов с ОПН, ассоциировались с отчетливым нарастанием риска ототоксичности данного препарата.
Системные гемодинамические нарушения являются доминирующей причиной ОТН, поэтому в основные задачи лечения входит стабилизация циркуляторных нарушений, АД и поддержание регионального почечного кровообращения.
Первая задача решается с помощью коррекции ОЦК и применения системных вазопрессоров. Областью применения вазопрессорных агентов, как правило, является шок чаще септической, реже - другой этиологии. Опубликованные к настоящему времени данные о применении использования вазопрессоров у больных с септическим шоком и преренальной ОПН пока не позволяют давать определенные рекомендации по использованию этой группы препаратов ни в отношении контроля системной гемодинамики, ни в отношении почечных эффектов.
На практике для лечения и предупреждения ОПН у тяжелых пациентов наиболее широко используется допамин в дозах 0,5-2 мкг/кг/мин (некоторые рекомендации предусматривают более высокие дозы - 1-5 мкг/кг/мин, предлагая в качестве «золотого стандарта» 3 мкг/кг/мин) в течение 6 часов.
В определенных ситуациях время инфузии допамина может быть увеличено, но обычно не более чем 24 ч. Возможные позитивные влияния допамина на течение ОПН связывают с увеличением почечного кровотока и снижением тубулярного транспорта Na через активацию DA1 рецепторов. Однако клинические испытания не обнаружили существенного значения инфузии допамина в профилактике и лечении ОТН, вероятно, в связи с активацией не только рецепторов DAl типа, но и других рецепторов (DA2 и адренергических), нивелирующих положительные эффекты первого для почечной гемодинамики и канальцевой реабсорбции натрия.
Не исключено, что фенолдапам, селективный агонист DA1 рецепторов, может оказаться более полезным в терапии ОТН.
Российским нефрологам данный препарат мало известен.
Существенных доказательств эффективности этой субстанции в терапии ОПН пока не представлено, поскольку результаты ряда исследований оказались противоречивыми.
Не разработаны и схемы его применения.
Например, для профилактики рентгено контрастой нефропатии его предлагают назначать за 15 мин-12 ч (!) до 0-12(!) ч после процедуры со скоростью 1 мкг/кг/ мин.
С другой стороны, как было показано в ряде исследований (в том числе двойных слепых, рандомизированных и плацебоконтролируемых), инфузия норадреналина более эффективна в отношении стабилизации системной гемодинамики по сравнению с допамином.
Теоретическая же вероятность нарушения регионарного кровообращения органов брюшной полости и почек за счет а адренергической стимуляции при применении норадреналина не нашла клинического подтверждения.
Применение адреналина показано в случаях, когда использование других прессорных агентов не дает желаемого увеличения АД.
Добутамин может быть эффективен в снижении риска внутрибольничной смертности при раннем назначении у больных с септическим шоком, однако не обнаружено его положительного влияния ни на диурез, ни на клиренс креатинина. На роль эффективного вазопрессора при преренальной ОПН может претендовать недавно вошедший в клиническую практику вазопрессин (АДГ), который в пилотных исследованиях при септическом шоке эффективно повышал системное АД, позволяя снижать дозировки или отменять другие прес сорные препараты.
В любом случае, необходимы проспективные исследования, которые смогли бы прояснить ситуацию с выбором вазопрессоров у данной весьма тяжелой категории больных. Поскольку специфическая терапия ОПН, связанная с воздействием нефротоксических агентов, практически не разработана, предотвращение нарушений функции почек является краеугольным камнем в ведении этих больных.
Основной принцип - профилактика за счет щадящего режима использования препаратов с учетом факторов риска, своевременная коррекция обрати- мых факторов риска и немедленная отмена препаратов в случае развития острого нарушения функции почек.
В ряде случаев рано начатые лечебно профилактические мероприятия могут предотвратить развитие и улучшить отдаленный прогноз ОПН.
 Нарушение функционирования почек, которое развивается стремительно и сопровождается болезненными ощущениями, получило название острая почечная недостаточность. Это серьезная патология, в результате которой происходит нарушение выработки и выделения мочи. Такие негативные изменения провоцируют ряд осложнений, которые неблагоприятно сказываются на общем состоянии, самочувствии и приводят к другим, более серьезным болезням. Крайне важно своевременно оказать помощь при первом проявлении заболевания и предотвратить перерождение острой формы в хроническую, которая будет сопровождать человека до конца его жизни, напоминая о себе обострениями, болями и другими симптомами. Начинать лечение медицинскими препаратами рекомендовано после тщательного обследования и проведения диагностики. Нередко с целью избавления от недуга пациенты прибегают к средствам народной медицины, которые также оказывают благоприятное воздействие на организм при острой форме почечной недостаточности.
Нарушение функционирования почек, которое развивается стремительно и сопровождается болезненными ощущениями, получило название острая почечная недостаточность. Это серьезная патология, в результате которой происходит нарушение выработки и выделения мочи. Такие негативные изменения провоцируют ряд осложнений, которые неблагоприятно сказываются на общем состоянии, самочувствии и приводят к другим, более серьезным болезням. Крайне важно своевременно оказать помощь при первом проявлении заболевания и предотвратить перерождение острой формы в хроническую, которая будет сопровождать человека до конца его жизни, напоминая о себе обострениями, болями и другими симптомами. Начинать лечение медицинскими препаратами рекомендовано после тщательного обследования и проведения диагностики. Нередко с целью избавления от недуга пациенты прибегают к средствам народной медицины, которые также оказывают благоприятное воздействие на организм при острой форме почечной недостаточности.
Что такое острая почечная недостаточность?
Острая почечная недостаточность – это патологическое нарушение работы почек, которое развивается быстро за несколько часов или дней и сопровождается рядом неприятных симптомов, интоксикацией организма и провоцирует появление разного рода осложнений. Основной причиной болезни является поражение почечной ткани или нарушение функционирования других внутренних органов.

В своем развитии болезнь проходит несколько стадий:
- Первый этап характеризуется минимальными патологическими изменениями в функционировании почек, снижением количества выделяемой мочи.
- Для второй стадии характерно значительное ухудшение работы почек, уменьшение объема мочи и сильное повышение токсических веществ в крови (креатинина). Из-за плохого вывода мочи происходит скопление жидкости в организме, что провоцирует отечность, развитие сердечных болезней, гипертонического криза.
- Третья стадия характеризуется отмиранием нефронов, заполнением мочевых протоков плазмой крови. Часто пациента мучает тахикардия, появляется шелушение кожи и ее сухость. В особо сложных случаях возможно впадение пациента в кому.
- Для заключительной стадии характерно восстановление функционирования почек, которое происходит крайне медленно и до полного выздоровления может пройти от 6 до 12 месяцев.
Причины заболевания
Почечная недостаточность в острой форме развивается под воздействием самых различных причин: от нарушения функционирования внутренних органов, до поражения ядами или механического поражения тканей почки. К наиболее распространенным и часто встречающимся факторам, провоцирующих заболевание, относится:
В зависимости от предпосылок, провоцирующие развитие болезни, острую почечную недостаточность можно подразделить на три типа:
- Преренальная ОПН – главным фактором развития является нарушение кровообращения почек или снижение скорости фильтрации, в результате чего значительно повышается уровень кретинина, происходит нарушение функционирования почек. При своевременно оказанной помощи болезнь хорошо поддается лечению, но в случае ее запущенной формы возможен некроз или ишемическая болезнь.
- Обструктивная ОПН – развитию данного вида заболевания способствует нарушение проходимости мочи в мочевыводящих путях. То есть почки свои функции выполняют в полной мере, но из-за поражения мочеточников моча не выделяется, что чаще всего бывает вызвано наличием опухолевых заболеваний, гематом или камней.
- Паренхиматозная ОПН – поражение почек, спровоцированное механическим, токсическим, химическим, ишемическим воздействием.
Симптомы острой почечной недостаточности
Синдром острой почечной недостаточности характеризуется следующими симптомами:
Диагностика заболевания
Перед тем как приступить к выбору лечения необходимо правильно установить диагноз и степень поражения почек. Прежде всего потребуется консультация и терапевта. При первом посещение кабинета врача он проводит тщательный осмотр, собирает анамнез, устанавливает возможные причины, которые могли спровоцировать болезнь. Для получения полной картины состояния здоровья пациента доктор назначает следующие диагностические процедуры:
Лечение острой почечной недостаточности
Устранение симптомов и причин острой почечной недостаточности зависит от стадии болезни, наличия осложнений и общего состояния здоровья пациента. Так, на первом этапе врачи ставят главную цель – устранение причины, спровоцировавшей заболевание, и основная терапия направлена на решение данной проблемы. Если у пациента наблюдается вторая или третья стадия, то лечение состоит в восстановлении функции почек и устранении всех осложнений.
Лечение ОПН направлено на:
- Устранение факторов, которые привели к нарушению функционирования почек.
- Восстановление нормальной работы органа.
- Нормализацию объема выделяемой мочи в сутки.
Для достижения поставленных целей врачи используют следующие методы лечения:
Профилактика почечной недостаточности
Для того чтобы предотвратить развитие острой почечной недостаточности необходимо вовремя устранить все факторы, которые могут спровоцировать заболевание: принимать лекарственные препараты под чутким контролем врача (особенно при наличии предрасположенности к данного рода заболеванию); своевременно получать помощь специалистов при отравлении ядами или химическими веществами; вовремя лечить дисфункции внутренних органов, которые могут спровоцировать ОПН; проходить профилактические осмотры.
Лечение острой почечной недостаточности необходимо начинать с терапии основного заболевания, её вызвавшего.
Для оценки степени задержки жидкости в организме пациента желательно ежедневное взвешивание. Для более точного определения степени гидратации, объема инфузионной терапии и показаний к ней необходима установка катетера в центральную вену. Следует также учитывать суточный диурез, а также артериальное давление больного.
При преренальной острой почечной недостаточности необходимо скорейшее восстановление ОЦК и нормализация артериального давления.
Для лечения ренальной острой почечной недостаточности, вызванной различными веществами лекарственной и нелекарственной природы, а также некоторыми заболеваниями, необходимо как можно раньше начать проведение детоксикационной терапии. Желательно учитывать молекулярную массу токсинов, вызвавших острую почечную недостаточность, и клиренсные возможности применяемого метода эфферентной терапии (плазмафереза, гемосорбции, гемодиафильтрации или гемодиализа), возможности наиболее раннего введения антидота.
При постренальной острой почечной недостаточности необходимо немедленное дренирование мочевывыводящих путей для восстановления адекватного оттока мочи. При выборе тактики оперативного вмешательства на почке в условиях острой почечной недостаточности ещё до операции необходима информация о достаточной функции контралатеральной почки. Больные с единственной почкой встречаются не так редко. Во время стадии полиурии, развивающейся, как правило, после дренирования, необходимо контролировать баланс жидкости в организме больного и электролитный состав крови. Полиурическая стадия острой почечной недостаточности может проявляться гипокалиемией.
Медикаментозное лечение острой почечной недостаточности
При ненарушенном пассаже по ЖКТ необходимо адекватное энтеральное питание. При его невозможности потребность в белках, жирах, углеводах, витаминах и минеральных веществах удовлетворяется с помощью внутривенного питания. С учётом выраженности нарушения клубочковой фильтрации потребление белка ограничивают до 20-25 г в сутки. Необходимая калорийность питания должна составлять не менее 1500 ккал/сут. Количество жидкости, необходимое больному, до развития полиурической стадии определяют, исходя из объёма диуреза за предыдущие сутки и дополнительных 500 мл.
Наибольшие сложности в лечении вызывает сочетание у пациента острой почечной недостаточности и уросепсиса. Сочетание сразу двух видов интоксикации уремической и гнойной - значительно усложняет лечение, а также значительно ухудшает прогноз в отношении жизни и выздоровления. При лечении этих больных необходимо применение эфферентных методов детоксикации (гемодиафильтрации, плазмафереза, непрямого электрохимического окисления крови), подбор антибактериальных препаратов по результатам бактериологического анализа крови и мочи, а также и их дозирование с учётом фактической клубочковой фильтрации.
Лечение больного гемодиализом (или модифицированным гемодиализом) не может служить противопоказанием к оперативному лечению заболеваний или осложнений, приведших к острой почечной недостаточности. Современные возможности мониторинга свёртывающей системы крови и её медикаментозной коррекции позволяют избежать риска кровоточивости во время операций и в послеоперационном периоде. Для проведения эфферентной терапии желательно использовать антикоагулянты короткого действия, например, гепарин натрия, избыток которого к концу лечения можно нейтрализовать антидотом - протамина сульфатом; в качестве коагулянта можно также использовать натрия цитрат. Для контроля свёртывающей системы крови обычно используют исследование активированного частичного тромбопластинового времени и определение количества фибриногена в крови. Метод определения времени свёртывания крови не всегда точен.
Лечение острой почечной недостаточностью еще до развития полиурической стадии требует назначения петлевых диуретиков, например фуросемида до 200-300 мг в сутки дробно.
Для компенсации процессов катаболизма назначают анаболические стероиды.
При гиперкалиемии показано внутривенное введение 400 мл 5% раствора глюкозы с 8 ЕД инсулина, а также 10-30 мл 10% раствора кальция глюконата. Если не удаётся корректировать гиперкалиемию консервативными методами, то больному показано проведение экстренного гемодиализа.
Оперативное лечение острой почечной недостаточности
Для замещения функции почек в период олигурии можно использовать любой метод очищения крови:
- гемодиализ;
- перитонеальный диализ;
- гемофильтрацию;
- гемодиафильтрацию;
- слабопоточную гемодиафильтрацию.
При полиорганной недостаточности лучше начинать со слабопоточной гемодиафильтрации.
Лечение острой почечной недостаточности: гемодиализ
Показания для проведения гемодиализа или его модификации при хронической и острой почечной недостаточности различны. При лечении острой почечной недостаточности частота, длительность процедуры, диализная нагрузка, величина фильтрации и состав диализата подбирают индивидуально на момент осмотра, перед каждым сеансом лечения. Лечение гемодиализом продолжают, не допуская повышения содержания мочевины в крови выше 30 ммоль/л. При разрешении острой почечной недостаточности концентрация креатинина крови начинает снижаться раньше, чем концентрация мочевины крови, что расценивают как положительный прогностический признак.
Экстренные показания для проведения гемодиализа (и его модификаций):
- «неуправляемая» гиперкалиемия;
- выраженная гипергидратация;
- гипергидратация лёгочной ткани;
- тяжёлая уремическая интоксикация.
Плановые показания для проведения гемодиализа:
- содержание мочевины в крови более 30 ммоль/л и/или концентрация креатинина, превышающая 0,5 ммоль/л;
- выраженные клинические признаки уремической интоксикации (такие, как уремическая энцефалопатия, уремические гастрит, энтероколит, гастроэнтероколит);
- гипергидратация;
- выраженный ацидоз;
- гипонатриемия;
- быстрое (в течение нескольких дней) нарастание содержания уремических токсинов в крови (суточный прирост содержания мочевины, превышающий 7 ммоль/л, и креатинина - 0.2-0.3 ммоль/л) и/или снижение диуреза
С наступлением стадии полиурии необходимость в лечении гемодиализом отпадает.
Возможные противопоказания к проведению эфферентной терапии:
- афибриногенемическое кровотечение;
- ненадёжный хирургический гемостаз;
- паренхиматозное кровотечение.
В качестве сосудистого доступа для проведения диализного лечения используют двухходовой катетер, установленный в одну из центральных вен (подключичную, ярёмную или бедренную).